题目内容
19.臭氧(O3)和汽车尾气造成的大气污染物NO发生如下反应:NO+O3=NO2+2O、NO2+O=NO+O2从反应过程和最终产物分析判断,NO是( )| A. | 氧化剂和还原产物 | B. | 还原剂和氧化产物 | ||
| C. | 氧化剂和催化剂 | D. | 还原剂和催化剂 |
分析 NO+O3═NO2+O2,NO2+O═NO+O2,将两个方程式相加,消除中间反应物,可得出总的化学方程式为O3+O=2O2从过程可以看出NO反应前后未变,只是参与化学反应的过程,这符合催化剂的特点,所以起到了催化剂的作用,据此分析解答.
解答 解:臭氧与大气污染物之一的NO发生反应:NO+O3═NO2+O2,在该反应中NO作还原剂,NO2+O═NO+O2,在该反应中NO作氧化产物,将两个方程式相加,合在一块是:O3+NO+O+NO2═NO2+O2+NO+O2 反应物和生成物中相同的要消去即:O3+O═2O2,由方程式可知一氧化氮参加了反应,但最后又生成了它,催化剂在化学反应前后质量和化学性质不变,说明NO是催化剂,在第一个反应中NO还作还原剂.
故选D.
点评 本题考查了催化剂的判别,掌握催化剂在化学反应前后质量和化学性质不变的特点是解答的关键,注意在反应物和生成物进行抵消时,必须是抵消相同分子数目的同种物质,题目难度不大.

练习册系列答案
相关题目
5.1g炭与适量的水蒸气反应生成CO和氢气,需要吸收10.93KJ的热量,则下列热化学方程式正确的是( )
| A. | C+H2O=CO+H2;△H=+131.2KJ/mol | |
| B. | CO(g)+H2(g)=C(s)+H2O(g);△H=-131.2KJ/mol | |
| C. | C(s)+H2O(g)=CO(g)+H2(g);△H=+10.93KJ/mol | |
| D. | C(s)+H2O(g)=CO(g)+H2(g);△H=-131.2KJ/mol |
10.下列实验操作或装置(略去部分夹持仪器)正确的是( )
| A. | 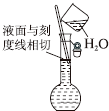 配制溶液 | B. | 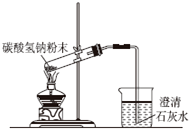 碳酸氢钠受热分解 | ||
| C. | 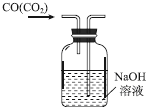 除去CO中的CO2 | D. | 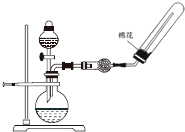 制备收集干燥的氨气 |
4.能正确表示下列反应的离子方程式是( )
| A. | 饱和碳酸氢钙溶液中加入饱和氢氧化钙溶液:Ca2++HCO3-+OH-=CaCO3↓+H2O | |
| B. | 氯化亚铁溶液中加入硝酸:Fe2++4H++NO3-=Fe3++2H2O+NO↑ | |
| C. | 氯气通入冷的氢氧化钠溶液中:2Cl2+2OH-=3Cl-+ClO-+H2O | |
| D. | 氨水中通入过量CO2:2NH3•H2O+CO2=2NH4++CO32-+H2O |
11.已知X元素原子的L电子层比Y元素原子的L电子层少2个电子,Y元素原子核外电子总数比X元素核外电子总数多3个,则下列说法不正确的是( )
| A. | X与Y能形成两种化合物,但化学键类型不相同 | |
| B. | Y与氢形成化合物YH,分子内存在离子键 | |
| C. | X与氢可形成化合物H2X2,分子内部存在极性键和非极性键 | |
| D. | Y2X2中阴、阳离子个数比1:2 |
9.下列各组物质中,互为同位素的是( )
| A. | T2O与D2O | B. | 4019K与4020Ca | ||
| C. | O2和O3 | D. | ${\;}_{6}^{12}$C和${\;}_{6}^{14}$C |
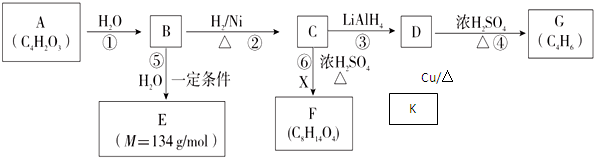
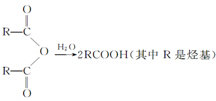 ②R-COOH$\stackrel{LiAlH_{4}}{→}$R-CH2OH(其中R是烃基)
②R-COOH$\stackrel{LiAlH_{4}}{→}$R-CH2OH(其中R是烃基)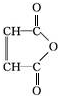 ;B中含氧官能团的名称是羧基;
;B中含氧官能团的名称是羧基;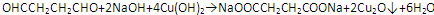
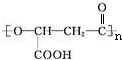 .有机物Y与E互为同分异构体,且具有相同的官能团种类和数目,则Y的结构可有2 种.
.有机物Y与E互为同分异构体,且具有相同的官能团种类和数目,则Y的结构可有2 种.