题目内容
14.已知反应:N2+3H2?2NH3 在一个容积为5L 的密闭容器中,装入2molN2和8molH2,在一定条件下反应5分钟后,测得NH3的浓度为0.5mol/L,求v(N2)、v(H2)、v(NH3).分析 反应速率v=$\frac{△c}{△t}$,化学反应速率之比等于化学计量数之比,据此计算即可.
解答 解:5分钟后,测得NH3的浓度为0.5mol/L,那么v(NH3)=$\frac{0.5mol/L}{5min}$=0.1mol/(L•min),
因为v(N2)=$\frac{1}{2}$v(NH3)=0.05mol/(L•min)
v(H2)=$\frac{3}{2}$v(NH3)=0.15 mol/(L•min),
答:v(N2)、v(H2)、v(NH3)分别为0.05mol/(L•min);0.15mol/(L•min);0.1mol/(L•min).
点评 本题主要考查的是化学反应速率的计算,正确掌握公式是解决本题的关键,还要注意化学计量数与反应速率的正比例关系,难度不大.

练习册系列答案
相关题目
5.电池是人类生产和生活中的重要能量来源,各式各样电池的发明是化学对人类的一项重大贡献,下列有关电池的叙述正确的是( )
| A. | 锌锰干电池工作一段时间后碳棒变细 | |
| B. | 氢氧燃料电池可将热能直接转变为电能 | |
| C. | 太阳能电池的主要材料是高纯度的二氧化硅 | |
| D. | 氢氧燃料电池工作时氢气在负极被氧化 |
2.2000年,国家药品监督管理局发布通告暂停使用和销售含苯丙醇胺的药品制剂.苯丙醇胺(英文缩写为PPA)结构简式如下: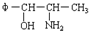 将φ-、H2N-、HO-在碳链上的位置作变换,可以写出多种同分异构体,共有多少种( )
将φ-、H2N-、HO-在碳链上的位置作变换,可以写出多种同分异构体,共有多少种( )
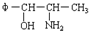 将φ-、H2N-、HO-在碳链上的位置作变换,可以写出多种同分异构体,共有多少种( )
将φ-、H2N-、HO-在碳链上的位置作变换,可以写出多种同分异构体,共有多少种( )| A. | 5 | B. | 7 | C. | 8 | D. | 9 |
9.下列反应不属于消去反应的是( )
| A. | CH3CH2OH$→_{170℃}^{浓硫酸}$CH2═CH2↑+H2O | |
| B. | CH3CHBrCH3+NaOH$→_{△}^{乙醇}$CH3CH═CH2↑+NaBr+H2O | |
| C. | 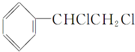 +2NaOH$→_{△}^{乙醇}$ +2NaOH$→_{△}^{乙醇}$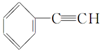 +2NaCl+2H2O +2NaCl+2H2O | |
| D. | 2CH3OH$→_{△}^{浓硫酸}$CH3-O-CH3+H2O |
19.臭氧(O3)和汽车尾气造成的大气污染物NO发生如下反应:NO+O3=NO2+2O、NO2+O=NO+O2从反应过程和最终产物分析判断,NO是( )
| A. | 氧化剂和还原产物 | B. | 还原剂和氧化产物 | ||
| C. | 氧化剂和催化剂 | D. | 还原剂和催化剂 |
6.某些电解质分子的中心原子最外层电子未达饱和结构,其电离采取结合溶液中其他离子的形式,而使中心原子最外层电子达到饱和结构.例如:硼酸分子的中心原子B最外层电子并未达到饱和,它在水中的电离过程为:
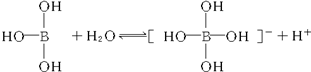
下列判断正确的是( )
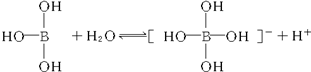
下列判断正确的是( )
| A. | 凡是酸或碱对水的电离都是抑制的 | |
| B. | 硼酸分子中除氢原子外每个其他原子最外层都满足8电子稳定结构 | |
| C. | 硼酸溶液与NaOH溶液反应的离子方程式为:H3BO3+OH-═[B(OH)4]- | |
| D. | 硼酸是两性化合物 |
3.向2L密闭容器里充入2mol M和一定量的N,发生如下反应:M(g)+2N(g)?E(g),当反应进行到4min时,测知M的浓度为0.2mol/L,则化学反应的平均速率( )
| A. | v(M)=0.4 mol/(L•min) | B. | v(N)=0.4 mol/(L•min) | ||
| C. | v(M)=0.8 mol/(L•min) | D. | v(E)=0.45 mol/(L•min) |
4.某烃0.1mol,在氧气中完全燃烧,生成13.2g CO2、7.2gH2O,则该烃的分子式为( )
| A. | 乙烯 | B. | 乙烷 | C. | 丙烯 | D. | 丙烷 |
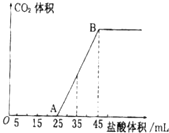 实验室欲配制0.1mol/L NaOH溶液并进行有关性质实验,请据此回答下列问题
实验室欲配制0.1mol/L NaOH溶液并进行有关性质实验,请据此回答下列问题