题目内容
19.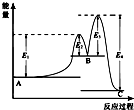 某反应由两步反应A═B═C构成,它的反应能量曲线如图所示(E1、E2、E3、E4表示活化能).下列有关叙述正确的是( )
某反应由两步反应A═B═C构成,它的反应能量曲线如图所示(E1、E2、E3、E4表示活化能).下列有关叙述正确的是( )| A. | A═B的反应热△H=+(E2-E1)KJ/mol | B. | 三种化合物中C最稳定 | ||
| C. | C═B 是放热反应 | D. | 整个反应中△H=E1-E4 |
分析 A→B的反应,反应物总能量小于生成物总能量,反应吸热,B→C的反应,反应物的总能量大于生成物总能量,反应为放热反应,结合能量的高低解答该题.
解答 解:A.A═B的反应,反应物总能量小于生成物总能量,反应吸热,△H=+(E1-E2)KJ/mol,故A错误;
B.物质的总能量越低,越稳定,由图象可知C能量最低最稳定,故B正确;
C.B═C的反应,反应物的总能量大于生成物总能量,反应为放热反应,所以C═B为吸热反应,故C错误;
D.整个反应中△H=(E1-E2)+(E2-E3)-E4=E1-E3-E4,故D错误.
故选B.
点评 本题考查化学反应与能量变化,题目难度不大,注意把握物质的总能量与反应热的关系,易错点为D,注意把握反应热的计算.

练习册系列答案
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案
相关题目
14.在下列各元素组中,除一种元素外,其余都可以按某种共性归属一类.请选出各组的例外元素,并将该组其他元素的可能归属按所给6种类型的编号填入表内.
归属类型:①主族元素 ②过渡元素③同周期元素 ④同族元素⑤金属元素 ⑥非金属元素.
| 元素组 | 例外元素 | 其他元素所属类型的编号 |
| (1)S、N、Na、Mg | N | ③ |
| (2)P、Sb、Si、As | Si | ④ |
| (3)Rb、B、Br、Fe | Fe | ① |
8.下列实验操作或装置正确的是( )
| A. |  利用图所示操作制备氢氧化铁胶体 | |
| B. | 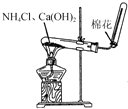 利用图所示装置制取NH3 | |
| C. |  利用图所示装置证明H2CO3酸性强于苯酚 | |
| D. |  利用图所示装置制备乙酸乙酯 |

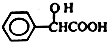 .工业上扁桃酸可以由烃A经过以下步骤合成得到:
.工业上扁桃酸可以由烃A经过以下步骤合成得到: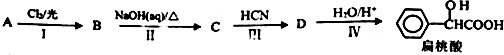
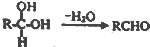
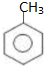 ;扁桃酸中含氧官能团名称羟基、羧基.
;扁桃酸中含氧官能团名称羟基、羧基. .
.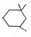 )在浓硫酸作用下反应生成,请写出反应的化学方程式
)在浓硫酸作用下反应生成,请写出反应的化学方程式
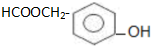 .
.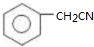 )为原料合成扁桃酸的同分异构体-对羟基苯乙酸(
)为原料合成扁桃酸的同分异构体-对羟基苯乙酸(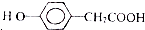 )的合理路线.
)的合理路线.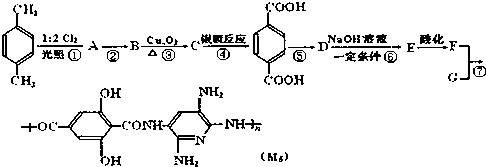
 ,
, ;F的含氧官能团的名称有羧基、(酚)羟基.
;F的含氧官能团的名称有羧基、(酚)羟基. .
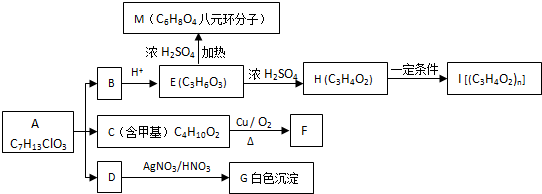
.

 +O2$→_{△}^{Cu}$
+O2$→_{△}^{Cu}$ +2H2O;②E→M:2HOCH2CH2COOH $→_{△}^{浓H_{2}SO_{4}}$
+2H2O;②E→M:2HOCH2CH2COOH $→_{△}^{浓H_{2}SO_{4}}$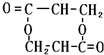 +2H2O;
+2H2O;