题目内容
16.已知:T℃温度下,0.1mol/L HB酸溶液的pH=3.T℃温度下,向0.1mol/L HB酸溶液中加入适当浓硫酸得到混合溶液R(滴入浓硫酸时忽略溶液体积的变化),若R溶液中c(SO42-)=0.05mol/L,则R溶液中c(B-)约为④(填序号)①0.1mol/L ②0.01mol/L ③1×10-4 mol/L ④1×10-5 mol/L.
分析 温度不变,HB的电离平衡常数不变,K=$\frac{c({H}^{+})•c({B}^{-})}{c(HB)}$=$\frac{1{0}^{-3}×1{0}^{-3}}{0.1-0.001}$=10-5,c(SO42-)=0.05mol/L,则硫酸电离出来的c(H+)=0.1mol/L,据此分析计算.
解答 解:向0.1mol/L HB酸溶液中加入适当浓硫酸,抑制了HB的电离,HB电离出来的氢离子和B离子浓度小于0.001mol/L,硫酸电离出来的c(H+)=0.1mol/L,HB的电离平衡常数不变,K=$\frac{c({H}^{+})•c({B}^{-})}{c(HB)}$=$\frac{1{0}^{-3}×1{0}^{-3}}{0.1-0.001}$=10-5不变,则有$\frac{c({B}^{-})×0.1}{0.1}$=10-5,所以从c(B-)=10-5,故答案为:④.
点评 本题考查了据电离平衡常数的计算,注意电离平衡常数只受温度影响,温度不变其值不变,题目难度不大.

练习册系列答案
相关题目
7.某工厂用CaSO4、NH3、H2O、CO2制备(NH4)2SO4,其工艺流程如图:

下列推断不合理的是( )

下列推断不合理的是( )
| A. | 往甲中通适量CO2有利于(NH4)2SO4生成 | |
| B. | 生成1 mol(NH4)2SO4至少消耗2 molNH3 | |
| C. | CO2可被循环利用 | |
| D. | NH3、CO2的通入顺序可以互换 |
1.下列实验操作中错误的是( )
| A. | 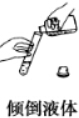 | B. | 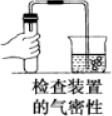 | C. | 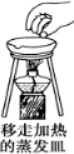 | D. | 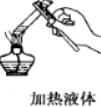 |
5.化学在生产和日常生活中有着重要的作用.下列说法中不正确的是( )
| A. | Na2FeO4能与水缓慢反应生成Fe(OH)3和O2,故可用作水的消毒剂和净化剂 | |
| B. | 钢铁表面烤蓝生成一层致密的Fe3O4,能起到防腐蚀作用 | |
| C. | 常温下氨能与氯气反应生成氯化氢和氮气,因此可用浓氨水检查氯气管道泄漏情况 | |
| D. | 开发利用可燃冰(固态甲烷水合物),有助于海洋生态环境的治理 |
 煤是重要的能源,也是生产化工产品的重要原料.试用所学知识,解答下列问题:
煤是重要的能源,也是生产化工产品的重要原料.试用所学知识,解答下列问题: