题目内容
下列化学用语表达正确的是( )
A、乙酸分子比例模型: | ||
B、原于核内有18个中于的氯原干:
| ||
C、铬原于价电子层排布图 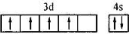 | ||
D、过氧化氢电子式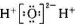 |
考点:球棍模型与比例模型,电子式、化学式或化学符号及名称的综合
专题:化学用语专题
分析:A.图为乙醛的比例模型;
B.氯原子的核电荷数为17,中子数为18的氯原子的质量数为35;
C.24Cr外围电子排布式3d54s1,然后写出价电子层排布图;
D.过氧化氢为共价化合物.
B.氯原子的核电荷数为17,中子数为18的氯原子的质量数为35;
C.24Cr外围电子排布式3d54s1,然后写出价电子层排布图;
D.过氧化氢为共价化合物.
解答:
解:A.乙酸分子比例模型: ,故A错误;
,故A错误;
B.核电荷数为17,中子数为18的氯原子为
Cl,故B正确;
C.24Cr外围电子排布式3d54s1,价电子层排布图: ,故C错误;
,故C错误;
D.过氧化氢为共价化合物,电子式为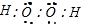 ,故D错误.
,故D错误.
故选B.
 ,故A错误;
,故A错误;B.核电荷数为17,中子数为18的氯原子为
35 17 |
C.24Cr外围电子排布式3d54s1,价电子层排布图:
 ,故C错误;
,故C错误;D.过氧化氢为共价化合物,电子式为
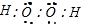 ,故D错误.
,故D错误.故选B.
点评:本题考查了比例模型、原子符号,电子排布图,电子式,注意掌握常见的化学用语的概念及表示方法,难度不大.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
为了探究锌与稀硫酸的反应速率[以v(H2)表示],向反应混合液中加入某些物质,下列判断错误的是( )
| A、加入KHSO4固体,v(H2)变大 |
| B、加入少量食盐水,v(H2)减小 |
| C、加入Na2CO3固体,v(H2)减小 |
| D、滴加少量CuSO4溶液,v(H2)减小 |
下列离子方程式书写正确的是( )
| A、硫酸氢钠溶液和过量的Ba(OH)2溶液反应:SO42-+H++Ba2++OH-═BaSO4↓+H2O |
| B、氧化铁溶于氢碘酸:Fe2O3+6H+═2Fe3++3H2O |
| C、过氧化钠固体与水反应:2O22-+2H2O═4OH-+O2↑ |
| D、将1mol?L-1的NaAlO2溶液和2.5mol?L-1的HCl溶液等体积均匀混合:AlO2-+H++H2O═Al(OH)3↓ |
下列物质中,不属于天然高分子化合物的是( )
| A、蛋白质 | B、淀粉 |
| C、纤维素 | D、油脂 |
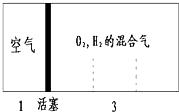 如图所示装置,室温下密闭容器内分别充入空气和H2、O2的混合气体在可移动的活塞两边,在标准状况下若将H2、O2的混合气体点燃引爆,活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央,则原来H2、O2的体积比最接近于( )
如图所示装置,室温下密闭容器内分别充入空气和H2、O2的混合气体在可移动的活塞两边,在标准状况下若将H2、O2的混合气体点燃引爆,活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央,则原来H2、O2的体积比最接近于( )①2:7 ②5:4 ③4:5 ④7:2.
| A、①② | B、③④ | C、②④ | D、①③ |
生活中处处有化学,下列表述不正确的是( )
| A、严禁乱弃废电池,防止重金属污染土壤和水源 |
| B、皮肤沾有苯酚时,立即用氢氧化钠稀溶液擦洗 |
| C、硅酸钠的水溶液俗称水玻璃,是制备硅胶和木材防火剂的原料 |
| D、用含有橙色的酸性重铬酸钾的仪器检验酒后驾车,利用了乙醇的挥发性和还原性 |
X、Y、Z、W为四种短周期非金属元素,其中X单质是一种重要的半导体材料,X、Y、Z同周期,且原子序数依次增大,Y、W同主族,离子半径Y2->W2-.下列说法正确的是( )
| A、X的非金属性比Y的强 |
| B、X和W组成的化合物化学性质活泼,与盐酸和氢氧化钠溶液都能反应 |
| C、Y的气态氢化物不如Z的气态氢化物稳定 |
| D、某溶液中通入Z的单质,再滴加淀粉溶液显蓝色,原溶液中一定含有I- |
下列有关实验说法中,错误的是( )
| A、葡萄糖银镜反应实验后的试管内壁附有银,可用氨水清洗 |
| B、酸碱中和滴定时,未用待测液润洗锥形瓶,对测定结果无影响 |
| C、向某溶液中加入足量盐酸无现象,再加入BaCl2溶液生成白色沉淀说明有SO42- |
| D、在无色溶液中先加入氯水、再加入CCl4,振荡静置,下层溶液显红棕色说明有Br- |