题目内容
下列有关实验说法中,错误的是( )
| A、葡萄糖银镜反应实验后的试管内壁附有银,可用氨水清洗 |
| B、酸碱中和滴定时,未用待测液润洗锥形瓶,对测定结果无影响 |
| C、向某溶液中加入足量盐酸无现象,再加入BaCl2溶液生成白色沉淀说明有SO42- |
| D、在无色溶液中先加入氯水、再加入CCl4,振荡静置,下层溶液显红棕色说明有Br- |
考点:葡萄糖的性质和用途,常见阴离子的检验,中和滴定
专题:实验评价题
分析:A.银不能与氨水反应,可以稀硝酸反应;
B.酸碱中和滴定时,不能用待测液润洗锥形瓶,否则相当多加待测液;
C.检验硫酸根离子应排除氯离子、碳酸根离子、亚硫酸根离子的干扰;
D.氯水中的氯气能够氧化溴离子生成单质溴,单质溴易溶于四氯化碳,四氯化碳密度大于水.
B.酸碱中和滴定时,不能用待测液润洗锥形瓶,否则相当多加待测液;
C.检验硫酸根离子应排除氯离子、碳酸根离子、亚硫酸根离子的干扰;
D.氯水中的氯气能够氧化溴离子生成单质溴,单质溴易溶于四氯化碳,四氯化碳密度大于水.
解答:
解:A.银不能与氨水反应,可以稀硝酸反应,葡萄糖银镜反应实验后的试管内壁附有银,可用稀硝酸清洗,故A错误;
B.酸碱中和滴定时,不能用待测液润洗锥形瓶,否则相当多加待测液,使得结果偏高,故B正确;
C.向某溶液中加入足量盐酸无现象,排除氯离子、碳酸根离子、亚硫酸根离子的干扰,再加入BaCl2溶液生成白色沉淀说明有SO42-,故C正确;
D.在无色溶液中先加入氯水,氯水中的氯气能够氧化溴离子生成单质溴,单质溴易溶于四氯化碳呈现红棕色,四氯化碳与水互补相溶,密度大于水,所以溶液分层溶有溴的四氯化碳在下层,故D正确;
故选:A.
B.酸碱中和滴定时,不能用待测液润洗锥形瓶,否则相当多加待测液,使得结果偏高,故B正确;
C.向某溶液中加入足量盐酸无现象,排除氯离子、碳酸根离子、亚硫酸根离子的干扰,再加入BaCl2溶液生成白色沉淀说明有SO42-,故C正确;
D.在无色溶液中先加入氯水,氯水中的氯气能够氧化溴离子生成单质溴,单质溴易溶于四氯化碳呈现红棕色,四氯化碳与水互补相溶,密度大于水,所以溶液分层溶有溴的四氯化碳在下层,故D正确;
故选:A.
点评:本题侧重考查实验的基础知识,明确实验的原理、各种物质的性质是解题关键,注意酸碱中和滴定的误差分析.

练习册系列答案
 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案
相关题目
下列说法错误的是( )
| A、MnO2、CuO、Fe三种物质的粉末都是黑色的,用浓盐酸不能将它们区别开 |
| B、虽然碘易溶于酒精而不易溶于水,但是不能用酒精来萃取碘水中的碘 |
| C、用湿润的KI淀粉试纸可以检验氯化氢气体中是否含有氯气 |
| D、用KSCN溶液可以检验硫酸亚铁溶液中是否含有铁离子 |
下列化学用语表达正确的是( )
A、乙酸分子比例模型: | ||
B、原于核内有18个中于的氯原干:
| ||
C、铬原于价电子层排布图 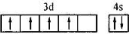 | ||
D、过氧化氢电子式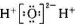 |
已知2SO2+O2?2SO3为放热反应,关于该反应的下列说法正确的是( )
| A、O2的能量一定高于SO2的能量 |
| B、因该反应为放热反应,故不必加热反应就可发生 |
| C、SO2的能量一定高于SO3的能量 |
| D、SO2和O2的总能量一定高于SO3的总能量 |
 19世纪丹麦学者尤利乌斯?托姆森得到一个计算CuCl2?2H2O在水中溶解热效应(设为△H,且当△H<0,放热;△H>0吸热)的式子,当所得溶液中1mol CuCl2有x mol水时,所产生的热效应△H=[3.35-21.02×
19世纪丹麦学者尤利乌斯?托姆森得到一个计算CuCl2?2H2O在水中溶解热效应(设为△H,且当△H<0,放热;△H>0吸热)的式子,当所得溶液中1mol CuCl2有x mol水时,所产生的热效应△H=[3.35-21.02×| (x-10) |
| x+11.24 |
| A、仅根据题中信息,无法计算出20℃时CuCl2饱和溶液的物质的量浓度 |
| B、当x<10,因CuCl2不能完全溶解,上图无物理意义 |
| C、在极稀的溶液中,1 mol CuCl2溶液时约放出17.67kJ热量 |
| D、CuCl2?2H2O溶于水是放热的 |
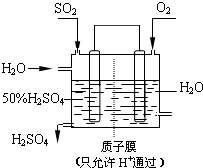 工业上生产硫酸时,利用催化氧化反应将SO2转化为SO3是一个关键步骤.
工业上生产硫酸时,利用催化氧化反应将SO2转化为SO3是一个关键步骤. 有如下化学反应:2A(g)+B(g)??2C(g)(正反应为放热反应).
有如下化学反应:2A(g)+B(g)??2C(g)(正反应为放热反应).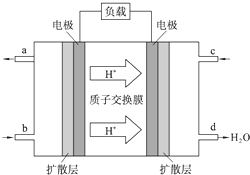 为了节能减排、缓解能源短缺,我国大力开发甲醇等可再生的新能源.工业上根据CO(g)+2H2(g)═CH3OH(g)△H合成甲醇.
为了节能减排、缓解能源短缺,我国大力开发甲醇等可再生的新能源.工业上根据CO(g)+2H2(g)═CH3OH(g)△H合成甲醇.