题目内容
生活中处处有化学,下列表述不正确的是( )
| A、严禁乱弃废电池,防止重金属污染土壤和水源 |
| B、皮肤沾有苯酚时,立即用氢氧化钠稀溶液擦洗 |
| C、硅酸钠的水溶液俗称水玻璃,是制备硅胶和木材防火剂的原料 |
| D、用含有橙色的酸性重铬酸钾的仪器检验酒后驾车,利用了乙醇的挥发性和还原性 |
考点:常见的生活环境的污染及治理,含硅矿物及材料的应用,乙醇的化学性质,苯酚的化学性质
专题:化学应用
分析:A、废电池中含有重金属,能污染土壤和水源;
B、氢氧化钠具有腐蚀性;
C、根据硅酸钠的用途;
D、根据乙醇的沸点低,易挥发,故可以易被检测,同时乙醇具有还原性,可被K2Cr2C7氧化来分析.
B、氢氧化钠具有腐蚀性;
C、根据硅酸钠的用途;
D、根据乙醇的沸点低,易挥发,故可以易被检测,同时乙醇具有还原性,可被K2Cr2C7氧化来分析.
解答:
解:A、严禁乱弃废电池,可防止重金属污染土壤和水源,故A正确;
B、氢氧化钠具有腐蚀性,苯酚可溶于酒精,可用酒精清洗,故B错误;
C、硅酸钠的水溶液俗称水玻璃,是制备硅胶和木材防火剂的原料,故C正确;
D、交警对驾驶员进行呼气酒精检测的原理是:橙色的K2Cr2O7酸性水溶液与乙醇迅速生成蓝绿色Cr3+,利用了乙醇的挥发性和还原性,故D正确;
故选B.
B、氢氧化钠具有腐蚀性,苯酚可溶于酒精,可用酒精清洗,故B错误;
C、硅酸钠的水溶液俗称水玻璃,是制备硅胶和木材防火剂的原料,故C正确;
D、交警对驾驶员进行呼气酒精检测的原理是:橙色的K2Cr2O7酸性水溶液与乙醇迅速生成蓝绿色Cr3+,利用了乙醇的挥发性和还原性,故D正确;
故选B.
点评:本题主要考查了重金属污染、物质的性质与用途,难度不大,注意掌握物质的性质.

练习册系列答案
 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案
相关题目
铅蓄电池是可充电型电池,电池总反应为:Pb+PbO2+2H2SO4
2PbSO4+2H2O,下列说法正确的是( )
| 放电 |
| 充电 |
| A、该蓄电池放电工作时SO42-向正极移动 |
| B、充电时阳极的电极反应式是Pb+SO42--2e-═PbSO4 |
| C、用铅蓄电池电解氯化钠溶液,当阳极上收集到11.2L氯气时(标况下),理论上负极板的质量增加48g |
| D、铅蓄电池为电解电源,当蓄电池中有0.4mol H+被消耗时,电路中通过的电子的物质的量为0.4mol |
下列对淀粉、纤维素的叙述正确的是( )
| A、它们的组成都是(C6H10O5)n,但n值不同,因此淀粉、纤维素互为同系物 |
| B、它们都不溶于水,在热水中颗粒会膨胀破裂,发生酯化作用 |
| C、它们都属于高分子化合物,一定条件下都可以水解,最终产物都是葡萄糖 |
| D、淀粉是还原性糖,纤维素是非还原性糖 |
分离苯和水混合物的操作方法是( )
| A、过滤 | B、分液 | C、萃取 | D、蒸馏 |
下列化学用语表达正确的是( )
A、乙酸分子比例模型: | ||
B、原于核内有18个中于的氯原干:
| ||
C、铬原于价电子层排布图 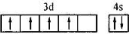 | ||
D、过氧化氢电子式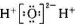 |
金刚石与石墨是碳的两种同素异形体,在100kPa时,1mol石墨转化为金刚石要吸收1.895kJ的热量,下列说法正确的是( )
| A、金刚石比石墨稳定 |
| B、1mol石墨比1mol金刚石的总能量低 |
| C、1mol石墨比1mol金刚石的总能量高 |
| D、石墨比金刚石稳定 |
已知2SO2+O2?2SO3为放热反应,关于该反应的下列说法正确的是( )
| A、O2的能量一定高于SO2的能量 |
| B、因该反应为放热反应,故不必加热反应就可发生 |
| C、SO2的能量一定高于SO3的能量 |
| D、SO2和O2的总能量一定高于SO3的总能量 |





