题目内容
7.某含苯环的化合物A,其相对分子质量为104,碳的质量分数为92.3%.(1)A的分子式为C8H8.
(2)A与溴的四氯化碳溶液反应的化学方程式为
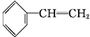 +Br2→
+Br2→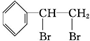 ,反应类型是加成反应.
,反应类型是加成反应.(3)一定条件下,A与氢气反应,得到的化合物中碳的质量分数为85.7%,写出此化合物的结构简式
 .
.(4)在一定条件下,由A聚合得到的高分子化合物的化学方程式为n
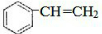 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$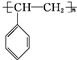 .
.
分析 (1)根据相对分子质量和含碳量可计算含氢量,进而计算C、H原子数目,可知分子式;
(2)该物质含有苯环,能与溴发生反应,说明A应为苯乙烯;
(3)一定条件下,A与氢气反应,可得乙苯或乙基环己烷,结合含氢量判断;
(4)含有C=C,可发生加聚反应生成聚苯乙烯.
解答 解:(1)1molA中n(C)=$\frac{104g×92.3%}{12g/mol}$=8mol,n(H)=$\frac{104g×(1-92.3%)}{1g/mol}$=8,则分子式为C8H8,故答案为:C8H8;
(2)该物质含有苯环,能与溴发生反应,说明A应为苯乙烯,结构为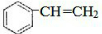 ,与溴发生加成反应生成
,与溴发生加成反应生成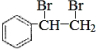 ,则反应的方程式为
,则反应的方程式为 +Br2→
+Br2→ ,
,
故答案为: +Br2→
+Br2→ ;加成反应;
;加成反应;
(3)一定条件下,A与氢气反应,可得乙苯或乙基环己烷,得到的化合物中碳的质量分数为85.7%,应为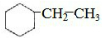 ,其中ω(C)=$\frac{12×8}{12×8+16}$×100%=85.7%,故答案为:
,其中ω(C)=$\frac{12×8}{12×8+16}$×100%=85.7%,故答案为: ;
;
(4)含有C=C,可发生加聚反应生成聚苯乙烯,即n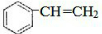 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$ ,故答案为:n
,故答案为:n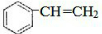 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$ .
.
点评 本题考查有机物的推断,为高频考点,侧重于学生的分析、计算能力的考查,题目难度中等,注意根据元素的含量和相对分子质量推断A为解答该题的关键,学习中注意有机物官能团的性质.

练习册系列答案
相关题目
17.短周期两种元素,它们的原子序数相差2,则( )
| A. | 可能同周期,也可能同主族 | B. | 若一种是F,另一种肯定是Na | ||
| C. | 若一种是Mg,另一种只能是硅 | D. | 一定同周期,不可能同主族 |
15.以下关于分子间作用力的叙述不正确的是( )
| A. | 分子间作用力是一种较弱的化学键 | |
| B. | 分子间作用力较弱,破坏它所需能量较少 | |
| C. | 分子间作用力对分子晶体的熔、沸点有影响 | |
| D. | 稀有气体分子间存在分子间作用力 |
2.根据下列各反应现象所归纳的元素性质不正确的是( )
| A. | 将一小块钠投入到盛有硫酸铜溶液的烧杯中,发现没有紫红色的铜析出,不能说明钠的金属性比铜弱 | |
| B. | 用湿润的淀粉碘化钾试纸放置在有氯气产生的导管上端,发现试纸变蓝,说明氯元素的非金属性比碘元素强 | |
| C. | 把H2S气体和Cl2在集气瓶中混合,一段时间后发现瓶壁有淡黄色固体析出,说明Cl的非金属性比S强 | |
| D. | 将0.1 mol Na、Mg、Al分别与足量稀盐酸反应,金属失去的电子数分别为0.1 mol、0.2 mol、0.3 mol,说明这三种金属的活泼性为:Al>Mg>Na |
12.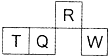 短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )
短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )
 短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )
短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )| A. | 最简单气态氢化物的热稳定性:R<Q | |
| B. | 最高价氧化物对应水化物的酸性:Q<W | |
| C. | 原子半径:T>Q>R | |
| D. | T的氧化物既能与强酸反应又能与强碱反应 |
19.元素在周期表中的位置,反映了元素的原子结构和元素的性质.
(1)下表是元素周期表的一部分,根据表中给出的8种元素,用元素符号或化学式回答下列问题:
①单质的化学性质最不活沷的元素是Ne;形成化合物种类最多的元素是C;原子半径最大的元素是Na.
②元素最高价氧化物对应水化物中,酸性最强的是HClO4.
③B与C两元素的气态氢化物,热稳定性较强的是第三周期VA族.
(2)四种短周期元素在周期表中的相对位置如图所示,其中Z元素原子核外电子总数是其最外层电子数的3倍.
回答下列问题:
①元素Z位于周期表中第三周期VA 族.
②Y元素的原子结构示意图为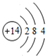 .
.
③元素X的气态氢化物与元素W的最高价氧化物对应水化物反应的生成物中化学键的类型是离子键、共价键.
(1)下表是元素周期表的一部分,根据表中给出的8种元素,用元素符号或化学式回答下列问题:
| 周期族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | A | B | C | D | ||||
| 3 | E | F | G | H |
②元素最高价氧化物对应水化物中,酸性最强的是HClO4.
③B与C两元素的气态氢化物,热稳定性较强的是第三周期VA族.
(2)四种短周期元素在周期表中的相对位置如图所示,其中Z元素原子核外电子总数是其最外层电子数的3倍.
| X | ||
| Y | Z | W |
①元素Z位于周期表中第三周期VA 族.
②Y元素的原子结构示意图为
 .
.③元素X的气态氢化物与元素W的最高价氧化物对应水化物反应的生成物中化学键的类型是离子键、共价键.
16.燃烧某有机物只生成二氧化碳8.8g和水2.7g,下列说法中,正确的是( )
| A. | 该有机物的最简式为C2H3 | |
| B. | 该有机物分子中肯定不含有碳碳叁键 | |
| C. | 该有机物不可能含有氧元素 | |
| D. | 该有机物不可能是丁烷 |
17.常温下,将盐酸和一元碱MOH溶液等体积混合(忽略溶液体积变化),两种溶液的浓度和混合后所得溶液的pH如下表:下列判断错误的是( )
| 实验编号 | 盐酸的浓度(mol?L-1) | MOH溶液的浓度(mol?L-1) | 混合溶液的pH |
| 甲 | 0.2 | 0.2 | a |
| 乙 | 0.2 | c1 | 7 |
| 丙 | 0.1 | 0.1 | 5 |
| A. | 甲组混合溶液中M+水解程度较丙组中大,且a<5 | |
| B. | 甲组混合溶液中:c(Cl-)>c(M+)>c(H+)>c(OH-) | |
| C. | 乙组混合溶液中:c(M+)+c(MOH)>0.1mol?L-1,且c1>0.2 | |
| D. | 丙组混合溶液中:c(OH-)+c(MOH)=1×10-5 mol?L-1 |
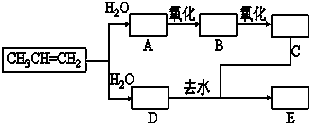 已知:①丙烯与水进行加成反应,其可能的产物有两种;②图中E为开链的酯类化合物,其分子式为C6H12O2.
已知:①丙烯与水进行加成反应,其可能的产物有两种;②图中E为开链的酯类化合物,其分子式为C6H12O2.