题目内容
17.如图是部分短周期元素原子半径与原子序数的关系图,下列说法不正确的是( )
| A. | N、Z两种元素的离子半径相比前者较大 | |
| B. | M、N两种元素的气态氢化物的稳定性相比后者较强 | |
| C. | X与M两种元素组成的化合物能与碱反应,但不能与任何酸反应 | |
| D. | X与Y两种元素组成的一种化合物中阴、阳离子的个数比为1:1 |
分析 图中元素分别为第二周期和第三周期元素的原子半径的变化,根据原子序数关系可知X为O元素,Y为Na元素,Z为Al元素,M为Si元素,N为Cl元素,结合对应物质的性质解答该题.
解答 解:图中元素分别为第二周期和第三周期元素的原子半径的变化,根据原子序数关系可知X为O元素,Y为Na元素,Z为Al元素,M为Si元素,N为Cl元素,
A.Z为Al元素,N为Cl元素,电子层结构相同,核电荷数越大离子半径越小,则离子半径Cl->Al3+,故A正确;
B.非金属性M(Si)<N(Cl),元素的非金属性越强,对应的氢化物越稳定,故N的氢化物较稳定,故B正确;
C.X与M两种元素组成的化合物为SiO2,能与氢氟酸反应,故C错误;
D.X与Y两种元素组成的化合物为氧化钠、过氧化钠,阴、阳离子的个数比为1:2,故D错误,
故选:CD.
点评 本题考查位置结构性质的关系及应用,难度中等,推断元素是解题的关键,要抓住“短周期主族元素”,根据原子半径变化规律结合原子序数进行推断.

练习册系列答案
相关题目
7.在人类已知的化合物中,种类最多的是( )
| A. | 过渡元素形成的化合物 | B. | ⅢA族元素形成的化合物 | ||
| C. | ⅣA族元素形成的化合物 | D. | ⅦA族元素形成的化合物 |
5.设NA为阿伏加德罗常数,下列叙述正确的是( )
| A. | 在常温常压下,22.4 L甲烷中含有原子数为5NA | |
| B. | 在标准状况下,2.24 L苯所含分子数为0.1NA | |
| C. | 28 g乙烯中含有碳碳双键的数目为NA | |
| D. | 1 mol-OH(羟基)与1 mol OH-所含有电子数相同,均为10NA |
12.观察图:对合成氨反应中,下列叙述错误的是( )
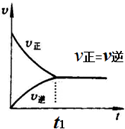

| A. | 开始反应时,正反应速率最大,逆反应速率为零 | |
| B. | 随着反应的进行,正反应速率逐渐减小,逆反应速率逐渐增大 | |
| C. | 反应到达t1时,正反应速率与逆反应速率相等,反应停止 | |
| D. | 反应在t1之后,正反应速率与逆反应速率相等,反应达到化学平衡状态 |
2.下列反应中,属于取代反应的是( )
| A. | CH4+2O2$\stackrel{点燃}{→}$ CO2+2H2O | B. | CH2=CH2+H2 $\stackrel{催化剂}{→}$ CH3-CH3 | ||
| C. |  | D. |  |
9.随着卤族元素原子序数递增,下列说法正确的是( )
| A. | 单质的熔、沸点逐渐降低 | |
| B. | 最高价氧化物对应水化物酸性逐渐减弱 | |
| C. | 单质的氧化性逐渐增强 | |
| D. | 气态氢化物的稳定性逐渐增强 |
6.在元素周期表中金属与非金属的分界处,可以找到( )
| A. | 农药 | B. | 催化剂 | C. | 半导体材料 | D. | 合金 |
7.下列叙述中,金属A的活泼性肯定比金属B的活泼性强的是( )
| A. | A是原子的主族序数比B原子的主族序数大 | |
| B. | A原子的周期序数B原子的周期序数大 | |
| C. | 1mol A与酸反应置换出的H2比1mol B与酸反应置换出的H2多 | |
| D. | 把AB用导线连接后放入盛有稀硫酸的烧杯中,B上产生气泡 |
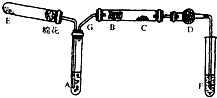 如图为某化学兴趣小组设计的乙醇氧化的实验装置(图中加热仪器、铁架台、铁夹等均未画出).图中:A为无水乙醇(沸点为78℃),B为绕成螺旋状的细铜丝或银丝,C为无水CuSO4粉末,D为碱石灰,F为新制的碱性Cu(OH)2悬浊液.
如图为某化学兴趣小组设计的乙醇氧化的实验装置(图中加热仪器、铁架台、铁夹等均未画出).图中:A为无水乙醇(沸点为78℃),B为绕成螺旋状的细铜丝或银丝,C为无水CuSO4粉末,D为碱石灰,F为新制的碱性Cu(OH)2悬浊液.