题目内容
10.实验室配制1mol•L-1盐酸250mL,下列不需用的仪器是( )| A. | 250 mL容量瓶 | B. | 托盘天平 | C. | 胶头滴管 | D. | 烧杯 |
分析 配制250mL 1mol/L盐酸的步骤为:计算、量取、稀释、冷却、移液、洗涤、定容、摇匀等,根据配制步骤选用仪器,然后判断不需要的仪器.
解答 解:根据配制250mL 1mol/L盐酸的步骤可知,需要使用的仪器为:量筒、烧杯、玻璃棒、250mL容量瓶、胶头滴管等,所以不需要的仪器为托盘天平,
故选B.
点评 本题考查了配制一定浓度的溶液中仪器的选用,题目难度不大,注意掌握配制一定物质的量浓度的溶液方法,明确配制过程中选用仪器的方法.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
15.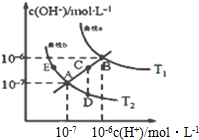 水的电离常数如图两条曲线所示,曲线中的点都符合c(H+)×c(OH-)=常数,下列说法错误的是( )
水的电离常数如图两条曲线所示,曲线中的点都符合c(H+)×c(OH-)=常数,下列说法错误的是( )
 水的电离常数如图两条曲线所示,曲线中的点都符合c(H+)×c(OH-)=常数,下列说法错误的是( )
水的电离常数如图两条曲线所示,曲线中的点都符合c(H+)×c(OH-)=常数,下列说法错误的是( )| A. | 图中温度T1>T2 | |
| B. | 图中五点Kw间的关系:B>C>A=D=E | |
| C. | 曲线a、b可以表示纯水的电离情况 | |
| D. | 若处在B点时,将pH=2的硫酸溶液与pH=11的KOH溶液等体积混合后,溶液显酸性 |
18. 在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
1.00.50t(s)123c(mol/L)abcd
(1)已知升高温度,NO2的浓度减小,则该反应是放热反应.
(2)图中表示NO2的变化的曲线是b
用O2表示从0~2s内该反应的平均速率v=0.15mol/(L•s)
(3)为使该反应的反应速率增大,且平衡向正反应方向移动的是c
a.及时分离除NO2气体 b.适当升高温度 c.增大O2的浓度 d.选择高效催化剂.
 在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 2.0 | 1.0 | 0.8 | 0.7 | 0.7 | 0.7 |
(1)已知升高温度,NO2的浓度减小,则该反应是放热反应.
(2)图中表示NO2的变化的曲线是b
用O2表示从0~2s内该反应的平均速率v=0.15mol/(L•s)
(3)为使该反应的反应速率增大,且平衡向正反应方向移动的是c
a.及时分离除NO2气体 b.适当升高温度 c.增大O2的浓度 d.选择高效催化剂.
5.对如图所示有机物分子的叙述错误的是( )
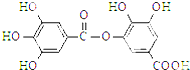

| A. | 能发生碱性水解,1 mol该有机物完全反应消耗8 mol NaOH | |
| B. | 常温下,能与Na2CO3溶液反应放出CO2 | |
| C. | 与稀硫酸共热,能生成两种有机物 | |
| D. | 该有机物的分子式为C14H10O9 |
15.下列物质的水溶液能导电,但属于非电解质的是( )
| A. | 食盐水 | B. | CO2 | C. | NaHCO3 | D. | 氢氧化钠 |
2.设nA为阿伏加德罗常数的值,下列说法中正确的是( )
| A. | 常温常压下,11.2 L氧气含有的分子数目为nA | |
| B. | 1 mol H2所含有的电子数目为nA | |
| C. | 4.4 g 二氧化碳含有的分子数目为0.1 nA | |
| D. | 1 mol/L CaCl2溶液中含有的氯离子数目为2nA |

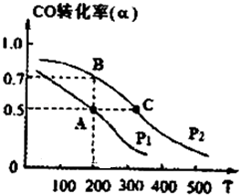 工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:CO(g)+2H2 (g)?CH3OH (g)△H=-116kJ/mol
工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:CO(g)+2H2 (g)?CH3OH (g)△H=-116kJ/mol