题目内容
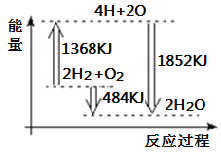
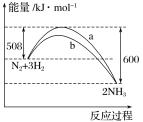
【题目】N2与H2反应生成NH3的过程中能量变化曲线如图所示。若在一个固定容积的密闭容器中充入1 mol N2和3 mol H2,使反应N2+3H2![]() 2NH3达到平衡,测得反应放出热量为Q1。
2NH3达到平衡,测得反应放出热量为Q1。
填写下列空白:
(1)Q1________92 kJ(填“>”“<”或“=”)。
(2)b曲线是________时的能量变化曲线。
(3)上述条件下达到平衡时H2的转化率为________。
(4)在温度体积一定的条件下,若通入2 mol N2和6 mol H2反应后放出的热量为Q2 kJ,则2Q1与Q2的关系为______________。
【答案】< 加入催化剂 Q1/92 Q2>2Q1
【解析】
(1)N2与H2反应生成NH3的反应为可逆反应,反应物不能完全转化为生成物;
(2)加催化剂降低反应的活化能;
(3)根据反应的热量之比等于物质的量之比求出参加反应的氢气的物质的量,再求出转化率;
(4)若通入2mol N2和6mol H2,则初始反应物的物质的量增大了一倍,由于压强增大平衡正向移动,所以反应的热量增大。
(1)由图可知反应的热化学方程式为:N2(g)+3H2(g)=2NH3(g)△H=508 kJ·mol-1-600 kJ·mol-1=-92kJ·mol-1,N2与H2反应生成NH3的反应为可逆反应,反应物不能完全转化为生成物,即1mol N2和3mol H2不能完全反应生成1molNH3,则反应放出的热量值Q1<92;
(2)加催化剂降低反应的活化能,所以图中b曲线表示加入了催化剂;
(3)设转化的氢气为xmol,则
N2(g)+3H2(g)=2NH3(g)△H=-92kJ·mol-1
3mol 92kJ
xmol Q1kJ
则x=3Q1/92 mol
所以达平衡时H2的转化率为3Q1/92mol÷3mol=Q1/92;
(4)向密闭容器中通入1mol N2和3mol H2,达到平衡时放出热量Q1kJ;另一容积相同的密闭容器中通入2mol N2和6mol H2,达到平衡时如果与原平衡相同,则放出热量应该是2QkJ,由于通入2mol N2和6mol H2的压强比通入1mol N2和3mol H2的大,平衡向正向移动,放出的热量还会增大,即Q2>2Q1。

 天天向上口算本系列答案
天天向上口算本系列答案【题目】草酸![]() 是一种重要的化工原料。某学习小组为探究草酸的性质,查阅了有关资料,草酸的部分性质如下表:
是一种重要的化工原料。某学习小组为探究草酸的性质,查阅了有关资料,草酸的部分性质如下表:
物质 | 性质 |
|
|
实验Ⅰ:根据图提供的仪器和试剂,设计实验证明草酸的受热分解产物中含有![]() 和
和![]() 部分夹持仪器和加热装置省略
部分夹持仪器和加热装置省略![]()
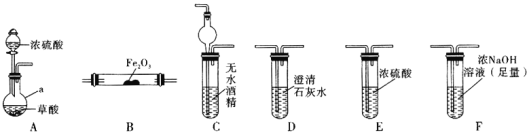
(1)仪器a的名称是_____________。
(2)各装置的正确连接顺序为![]() 装置可重复使用
装置可重复使用![]() ________
________![]() ________
________![]() ________
________![]() ________
________![]() 尾气处理。________________
尾气处理。________________
(3)用图中装置C的作用是____________________________。
(4)连接好装置进行的实验时,要先加热________![]() 填“A”“B”“C”“D”“E”或“F”
填“A”“B”“C”“D”“E”或“F”![]() 装置,能证明分解产物中有CO的实验依据是___________________。
装置,能证明分解产物中有CO的实验依据是___________________。
(5)某同学查阅资料发现,用氯化钯![]() 磷钼酸溶液可检验一氧化碳。一氧化碳与氯化钯溶液反应,生成了黑色的金属钯
磷钼酸溶液可检验一氧化碳。一氧化碳与氯化钯溶液反应,生成了黑色的金属钯![]() 固体,反应的化学方程式是___________________________。
固体,反应的化学方程式是___________________________。
实验 Ⅱ:草酸与甲醇在浓硫酸存在下酯化生成草酸二甲酯。反应为![]()
![]()
![]() 。在装有搅拌器、分水器的反应瓶中,加入草酸
。在装有搅拌器、分水器的反应瓶中,加入草酸![]() ,无水甲醇
,无水甲醇![]() ,苯
,苯![]() ,浓硫酸
,浓硫酸![]() ,搅拌下加热回流共沸脱水20小时,后转移到烧杯中冷却,按如图所示流程提纯。
,搅拌下加热回流共沸脱水20小时,后转移到烧杯中冷却,按如图所示流程提纯。
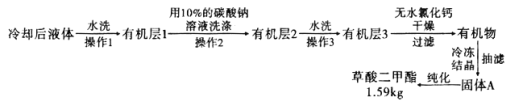
(6)![]() 提纯过程中用
提纯过程中用![]() 的碳酸钠溶液洗涤的作用是__________________________。
的碳酸钠溶液洗涤的作用是__________________________。
![]() 流程中纯化的方法为________________。
流程中纯化的方法为________________。
![]() 产率为____________
产率为____________![]() 精确到
精确到![]() 。
。
【题目】下列实验操作与预期实验目的或所得实验结论一致的是( )
选项 | 实验操作 | 实验目的或结论 |
A | 向废FeCl3蚀刻液X中加入少量的铁粉,振荡,未出现红色固体 | X中一定不含Cu2+ |
B | 向AgCl悬浊液中滴入少量KI溶液,有黄色沉淀生成 | 说明Ksp(AgCl)>Ksp(AgI) |
C | 制备乙酸乙酯的实验,将蒸出的乙酸乙酯蒸汽导在饱和的NaOH溶液液面以上 | 防止倒吸,便于分层 |
D | 向某溶液中滴加氯水,再滴加KSCN溶液,溶液变成红色 | 该溶液中一定含有Fe2+ |
A.AB.BC.CD.D
【题目】某兴趣小组的同学对一批铁的样品(含有杂质,杂质不溶于水,也不与稀硫酸反应)进行分析,甲、乙、丙三位同学分别进行实验,其中一位同学所用的稀硫酸与铁样品恰好完全反应,实验数据如下表:
甲 | 乙 | 丙 | |
烧杯+稀硫酸的质量/g | 200 | 150 | 150 |
加入铁的样品的质量/g | 9 | 9 | 14 |
充分反应后,烧杯+剩余物的质量/g | 208.7 | 158.7 | 163.7 |
请你认真分析数据,回答下列问题:
(1)哪位同学所用的稀硫酸与铁的样品恰好完全反应_____?
(2)计算铁的样品中铁的质量分数_____。