题目内容
【题目】草酸![]() 是一种重要的化工原料。某学习小组为探究草酸的性质,查阅了有关资料,草酸的部分性质如下表:
是一种重要的化工原料。某学习小组为探究草酸的性质,查阅了有关资料,草酸的部分性质如下表:
物质 | 性质 |
|
|
实验Ⅰ:根据图提供的仪器和试剂,设计实验证明草酸的受热分解产物中含有![]() 和
和![]() 部分夹持仪器和加热装置省略
部分夹持仪器和加热装置省略![]()
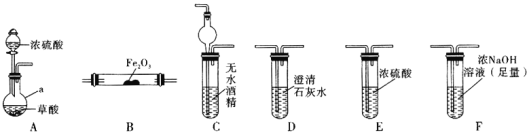
(1)仪器a的名称是_____________。
(2)各装置的正确连接顺序为![]() 装置可重复使用
装置可重复使用![]() ________
________![]() ________
________![]() ________
________![]() ________
________![]() 尾气处理。________________
尾气处理。________________
(3)用图中装置C的作用是____________________________。
(4)连接好装置进行的实验时,要先加热________![]() 填“A”“B”“C”“D”“E”或“F”
填“A”“B”“C”“D”“E”或“F”![]() 装置,能证明分解产物中有CO的实验依据是___________________。
装置,能证明分解产物中有CO的实验依据是___________________。
(5)某同学查阅资料发现,用氯化钯![]() 磷钼酸溶液可检验一氧化碳。一氧化碳与氯化钯溶液反应,生成了黑色的金属钯
磷钼酸溶液可检验一氧化碳。一氧化碳与氯化钯溶液反应,生成了黑色的金属钯![]() 固体,反应的化学方程式是___________________________。
固体,反应的化学方程式是___________________________。
实验 Ⅱ:草酸与甲醇在浓硫酸存在下酯化生成草酸二甲酯。反应为![]()
![]()
![]() 。在装有搅拌器、分水器的反应瓶中,加入草酸
。在装有搅拌器、分水器的反应瓶中,加入草酸![]() ,无水甲醇
,无水甲醇![]() ,苯
,苯![]() ,浓硫酸
,浓硫酸![]() ,搅拌下加热回流共沸脱水20小时,后转移到烧杯中冷却,按如图所示流程提纯。
,搅拌下加热回流共沸脱水20小时,后转移到烧杯中冷却,按如图所示流程提纯。
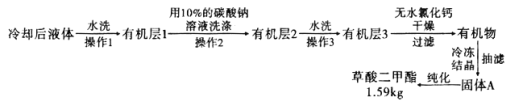
(6)![]() 提纯过程中用
提纯过程中用![]() 的碳酸钠溶液洗涤的作用是__________________________。
的碳酸钠溶液洗涤的作用是__________________________。
![]() 流程中纯化的方法为________________。
流程中纯化的方法为________________。
![]() 产率为____________
产率为____________![]() 精确到
精确到![]() 。
。
【答案】圆底烧瓶 ![]() 除去
除去![]() 中的草酸
中的草酸 ![]() 装置B中红色氧化铁变黑,装置D的澄清石灰水变浑浊
装置B中红色氧化铁变黑,装置D的澄清石灰水变浑浊 ![]() 除去硫酸
除去硫酸![]() 或硫酸、草酸和甲醇
或硫酸、草酸和甲醇![]() 重结晶
重结晶 ![]()
【解析】
![]() 根据装置图回答仪器a名称。
根据装置图回答仪器a名称。
![]() 为证明草酸的受热分解产物中含有
为证明草酸的受热分解产物中含有![]() 和CO,先将混合气体通入无水酒精除去升华出来的草酸,再通入澄清的石灰水检验二氧化碳,如果澄清的石灰水变浑浊,则证明含有二氧化碳气体,再用氢氧化钠溶液吸收二氧化碳,再将洗涤后的气体进行干燥,然后将气体再通过盛有红色氧化铁的装置,一氧化碳和红色的氧化铁反应生成铁和二氧化碳,再用澄清的石灰水检验二氧化碳是否存在,如果澄清石灰水变浑浊,则证明该混合气体中含有一氧化碳。
和CO,先将混合气体通入无水酒精除去升华出来的草酸,再通入澄清的石灰水检验二氧化碳,如果澄清的石灰水变浑浊,则证明含有二氧化碳气体,再用氢氧化钠溶液吸收二氧化碳,再将洗涤后的气体进行干燥,然后将气体再通过盛有红色氧化铁的装置,一氧化碳和红色的氧化铁反应生成铁和二氧化碳,再用澄清的石灰水检验二氧化碳是否存在,如果澄清石灰水变浑浊,则证明该混合气体中含有一氧化碳。
![]() 根据表格知,草酸
根据表格知,草酸![]() 时开始升华,草酸和氢氧化钙反应生成的草酸钙不溶于水,所以制取的气体中含有草酸蒸气而干扰二氧化碳的检验,要检验二氧化碳首先要除去草酸蒸气。
时开始升华,草酸和氢氧化钙反应生成的草酸钙不溶于水,所以制取的气体中含有草酸蒸气而干扰二氧化碳的检验,要检验二氧化碳首先要除去草酸蒸气。
![]() 一氧化碳和氧气的比例在一定范围内易产生爆炸,为防止产生安全事故发生,应先用生成的气体除去装置中的氧气;一氧化碳具有还原性,能还原红色的氧化铁生成铁单质,且生成二氧化碳。
一氧化碳和氧气的比例在一定范围内易产生爆炸,为防止产生安全事故发生,应先用生成的气体除去装置中的氧气;一氧化碳具有还原性,能还原红色的氧化铁生成铁单质,且生成二氧化碳。
![]() 一氧化碳与氯化钯溶液反应,生成了黑色的金属钯
一氧化碳与氯化钯溶液反应,生成了黑色的金属钯![]() 粉末,一氧化碳被氧化为
粉末,一氧化碳被氧化为![]() ,氯化钯中的氯元素变为HCl;
,氯化钯中的氯元素变为HCl;
![]() 酯化反应后的混合液体中除了草酸二甲酯外,还有草酸、甲醇、硫酸与水,先水洗除去大部分的硫酸、草酸和甲醇,有机层再用
酯化反应后的混合液体中除了草酸二甲酯外,还有草酸、甲醇、硫酸与水,先水洗除去大部分的硫酸、草酸和甲醇,有机层再用![]() 的碳酸钠溶液洗涤再除去全部的硫酸、草酸和甲醇,再次用水洗除去残留的碳酸钠,其中每一步的操作都是分液。纯化方法为重结晶。根据题意可知反应中甲醇过量,应用草酸计算产率。
的碳酸钠溶液洗涤再除去全部的硫酸、草酸和甲醇,再次用水洗除去残留的碳酸钠,其中每一步的操作都是分液。纯化方法为重结晶。根据题意可知反应中甲醇过量,应用草酸计算产率。
![]() 根据仪器a结构可得a为圆底烧瓶。
根据仪器a结构可得a为圆底烧瓶。
![]() 为证明草酸的受热分解产物中含有
为证明草酸的受热分解产物中含有![]() 和CO,先将混合气体通入无水酒精除去升华出来的草酸,再通入澄清的石灰水检验二氧化碳,如果澄清的石灰水变浑浊,则证明含有二氧化碳气体,再用氢氧化钠溶液吸收二氧化碳,再将洗涤后的气体进行干燥,然后将气体再通过盛有红色氧化铁的装置,一氧化碳和红色的氧化铁反应生成铁和二氧化碳,再用澄清的石灰水检验二氧化碳是否存在,如果澄清石灰水变浑浊,则证明该混合气体中含有一氧化碳,所以其排序是
和CO,先将混合气体通入无水酒精除去升华出来的草酸,再通入澄清的石灰水检验二氧化碳,如果澄清的石灰水变浑浊,则证明含有二氧化碳气体,再用氢氧化钠溶液吸收二氧化碳,再将洗涤后的气体进行干燥,然后将气体再通过盛有红色氧化铁的装置,一氧化碳和红色的氧化铁反应生成铁和二氧化碳,再用澄清的石灰水检验二氧化碳是否存在,如果澄清石灰水变浑浊,则证明该混合气体中含有一氧化碳,所以其排序是![]() 尾气处理。
尾气处理。
![]() 根据表格知,草酸
根据表格知,草酸![]() 时开始升华,草酸和氢氧化钙反应生成的草酸钙不溶于水,二氧化碳和氢氧化钙反应也生成碳酸钙沉淀,所以制取的气体中含有草酸蒸气而干扰二氧化碳的检验,要检验二氧化碳首先要除去草酸蒸气,所以C的作用是除去
时开始升华,草酸和氢氧化钙反应生成的草酸钙不溶于水,二氧化碳和氢氧化钙反应也生成碳酸钙沉淀,所以制取的气体中含有草酸蒸气而干扰二氧化碳的检验,要检验二氧化碳首先要除去草酸蒸气,所以C的作用是除去![]() 中的草酸。
中的草酸。
![]() 一氧化碳和氧气反应在一定范围内易产生爆炸,为防止产生安全事故发生,应先用生成的气体除去装置中的氧气,所以应先加热A后加热B;一氧化碳具有还原性,能还原红色的氧化铁生成铁单质和二氧化碳,二氧化碳能使澄清石灰水变浑浊,所以反应现象是装置B中红色氧化铁变黑,装置D的澄清石灰水变浑浊。
一氧化碳和氧气反应在一定范围内易产生爆炸,为防止产生安全事故发生,应先用生成的气体除去装置中的氧气,所以应先加热A后加热B;一氧化碳具有还原性,能还原红色的氧化铁生成铁单质和二氧化碳,二氧化碳能使澄清石灰水变浑浊,所以反应现象是装置B中红色氧化铁变黑,装置D的澄清石灰水变浑浊。
![]() 一氧化碳与氯化钯溶液反应,生成了黑色的金属钯
一氧化碳与氯化钯溶液反应,生成了黑色的金属钯![]() 粉末,一氧化碳被氧化为
粉末,一氧化碳被氧化为![]() ,氯化钯中的氯元素变为HCl,反应的化学方程式是
,氯化钯中的氯元素变为HCl,反应的化学方程式是![]() 。
。
![]() 酯化反应后的混合液体中除了草酸二甲酯外,还有草酸、甲醇、硫酸与水,先水洗除去大部分的硫酸、草酸和甲醇,有机层再用
酯化反应后的混合液体中除了草酸二甲酯外,还有草酸、甲醇、硫酸与水,先水洗除去大部分的硫酸、草酸和甲醇,有机层再用![]() 的碳酸钠溶液洗涤再除去全部的硫酸、草酸和甲醇,再次用水洗除去残留的碳酸钠,其中每一步的操作都是分液。
的碳酸钠溶液洗涤再除去全部的硫酸、草酸和甲醇,再次用水洗除去残留的碳酸钠,其中每一步的操作都是分液。
![]() 纯化方法为重结晶。
纯化方法为重结晶。
![]() 根据题意可知反应中甲醇过量,应用草酸计算,根据方程式可知,
根据题意可知反应中甲醇过量,应用草酸计算,根据方程式可知,![]() 的草酸理论上应生成
的草酸理论上应生成![]() 草酸二甲酯,草酸二甲酯的质量为
草酸二甲酯,草酸二甲酯的质量为![]() g,产率
g,产率![]() 。
。

【题目】某研究性学习小组利用H2C2O4溶液和酸性KMnO4溶液之间的反应来探究“外界条件改变对化学反应速率的影响”,实验如下:
实验 序号 | 实验温 度/K | 参加反应的物质 | 溶液颜色褪至无色时所需时间/s | ||||
KMnO4溶 液(含硫酸) | H2C2O4溶液 | H2O | |||||
V/mL | c/mol·L-1 | V/mL | c/mol·L-1 | V/mL | |||
A | 293 | 2 | 0.02 | 4 | 0.1 | 0 | t1 |
B | T1 | 2 | 0.02 | 3 | 0.1 | V1 | 8 |
C | 313 | 2 | 0.02 | V2 | 0.1 | 1 | t1 |
(1)通过实验A、B,可探究出_____(填外部因素)的改变对反应速率的影响,其中V1=_____,T1=______;通过实验________可探究出温度变化对化学反应速率的影。
(2)若t1<8,则由此实验可以得出的结论是_________;利用实验B中数据计算,用KMnO4的浓度变化表示的反应速率为v(KMnO4)=______。
(3)该反应中有无色无味气体产生且锰被还原为Mn2+,写出相应反应的离子方程式__________。
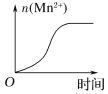
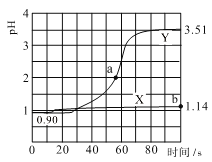
(4)该小组的一位同学通过查阅资料发现,上述实验过程中n(Mn2+)随时间变化的趋势如图所示,并认为造成此种变化的原因是反应体系中的某种粒子对KMnO4与草酸之间的反应有某种特殊的作用,则该作用是___________,相应的粒子最可能是(填序号)______。
【题目】硝基苯是一种重要有机合成中间体,实验室可用如下反应制备:![]() +HNO3
+HNO3![]()
![]() +H2O △H<0,已知该反应在温度稍高的情况下会生成间二硝基苯。有关数据如下表:
+H2O △H<0,已知该反应在温度稍高的情况下会生成间二硝基苯。有关数据如下表:
物质 | 苯 | 硝基苯 | 间二硝基苯 | 浓硝酸 | 浓硫酸 |
沸点/℃ | 80 | 211 | 301 | 83 | 338 |
溶解性 | 微溶于水 | 难溶于水 | 微溶于水 | 易溶于水 | 易溶于水 |
下列说法不正确的是( )
A.分液后的有机层,采用蒸馏的方法可将硝基苯首先分离出来
B.制备硝基苯的反应类型为取代反应
C.该反应温度控制在50~60℃的原因是减少反应物的挥发和副产物的生成
D.采用加入NaOH溶液、水洗涤、以及分液的方法可除去粗硝基苯中混有的无机杂质