题目内容
1.钾在周期表中第四周期,与钠同属IA族元素.请据此填空:(1)钾的离子结构示意图:
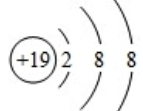 ;
;(2)金属钾与水反应的现象:浮在水面,熔成一个银白色的小球,不停游动,并发生着火燃烧或轻微的爆炸;往反应后的溶液中滴入酚酞,溶液变为红色.反应的化学方程式:2K+2H2O=2KOH+H2↑;
(3)碱性比较:NaOH<KOH(填“<”“>”“=”).
分析 (1)钾离子有19个质子,18个电子;
(2)钾与水反应生成氢氧化钾和氢气;
(3)同主族元素从上到下金属性依次增强,最高价氧化物对应水化物碱性依次增强.
解答 解:(1)钾离子有19个质子,18个电子.钾的离子结构示意图: ;
;
故答案为: ;
;
(2)钾与水反应生成氢氧化钾和氢气,溶液呈碱性,使酚酞变红,化学方程式:2K+2H2O=2KOH+H2↑;
故答案为:红;2K+2H2O=2KOH+H2↑;
(3)钠与钾同主族,钾位于钠的下方,金属性强于钠,所以氢氧化钾碱性强于氢氧化钠;
故答案为:<.
点评 本题考查了碱金属原子结构及性质,熟悉同主族元素性质的相似性和递变性是解题关键,题目难度不大.

练习册系列答案
相关题目
6.下列操作不能在石英坩埚中进行的是( )
| A. | 加热分解NaHCO3 | B. | 加热硫酸铜晶体 | C. | 熔化烧碱 | D. | 加热氯酸钾 |
13.自来水可用氯气消毒,某学生用这种自来水去配制下列物质溶液,不会产生明显的药品变质问题的是( )
| A. | NaNO3 | B. | FeCl2 | C. | Na2SO3 | D. | NaOH |
10.下列说法中正确的是( )
| A. | C60气化和I2升华克服的作用力相同 | |
| B. | 甲酸甲酯和乙酸的分子式相同,它们的熔点相近 | |
| C. | 氯化钠和氯化氢溶于水时,破坏的化学键都是离子键 | |
| D. | 用作高温结构陶瓷材料的固体是分子晶体 |
11.某CuCl2、FeCl3、HCl的混合液100ml,已知溶液中阳离子的浓度相同(不考虑水解),且Cl-的物质的量浓度为6mol/L,则此溶液最多溶解铁粉的质量为( )
| A. | 11.2g | B. | 5.6g | C. | 33.6g | D. | 22.4g |
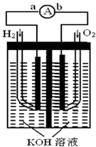 氢氧燃料电池是符合绿色化学理念的新型发电装置.如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:
氢氧燃料电池是符合绿色化学理念的新型发电装置.如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答: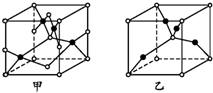 已知A、B、C、D、E五种元素的原子序数依次增大,其中A原子所处的周期数、族序数都与其原子序数相等;B原子核外电子有6种不同的运动状态;D原子L电子层上有2对成对电子;E+原子核外有3层电子且各层均处于全满状态.
已知A、B、C、D、E五种元素的原子序数依次增大,其中A原子所处的周期数、族序数都与其原子序数相等;B原子核外电子有6种不同的运动状态;D原子L电子层上有2对成对电子;E+原子核外有3层电子且各层均处于全满状态. .
.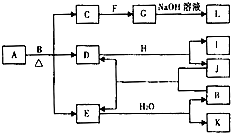 由两种元素组成的化合物A存在如图所示的转化关系(部分产物及反应条件已略去).已知:E为红棕色气体,F、H为金属单质,J为黑色非金属单质.L露置于空气中时,由白色最终转化为红褐色,B与F反应时可生成C,也可生成G.试回答下列问题:
由两种元素组成的化合物A存在如图所示的转化关系(部分产物及反应条件已略去).已知:E为红棕色气体,F、H为金属单质,J为黑色非金属单质.L露置于空气中时,由白色最终转化为红褐色,B与F反应时可生成C,也可生成G.试回答下列问题: