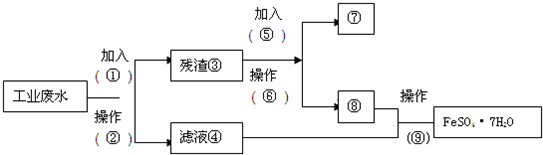
题目内容
1.(Ⅰ)下列操作会导致实验结果偏高的是D.A.配制一定物质的量浓度的硫酸溶液时,定容摇匀后,发现液面低于刻度线
B.在配制一定物质的量浓度溶液时,用10mL的量筒量取5.0mL液体溶质时俯视读数
C.用天平称量20.5g某物质,砝码和药品的位置放反,所得药品的质量
D.配制一定物质的量浓度的溶液时,定容时俯视读数,所得溶液的浓度
(Ⅱ)现有下列仪器或用品:
a铁架台(含铁圈、铁夹);b锥形瓶;c滴定管;d烧杯(若干);e玻璃棒;f胶头滴管;g托盘天平(含砝码);h滤纸;i量筒;j漏斗;k温度计
现有下列试剂:
A.NaOH固体 B.碳酸钠溶液 C.氯化镁溶液 D.蒸馏水
试填空:
(1)如图分别是温度计、量筒、滴定管的一部分,下述判断及读数(虚线刻度)不正确的是ABD.
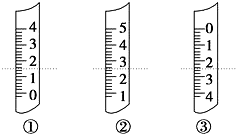
A.①是量筒,读数为1.5mL
B.②是量筒,读数为2.50mL
C.③是滴定管,读数为2.50mL
D.①是温度计,读数是1.50℃
(2)配制100mL 0.1mol•L-1的氢氧化钠溶液时,还缺少的仪器有药匙和100mL容量瓶.
(3)除去Mg(OH)2中混有的少量Ca(OH)2,可以用到的试剂是C(选填序号),操作方法是取样品加入蒸馏水溶解,、再加适量氯化镁溶液,充分反应后过滤、洗涤.
完成上述操作,上述仪器或用品用到的有a铁架台(含铁圈、铁夹)、d烧杯(若干)、e玻璃棒、f胶头滴管、h滤纸、i漏斗(从上述仪器或用品中选择,填上相应序号).
分析 (Ⅰ)A、部分溶液在刻度线上方,不影响配制溶液的结果;
B、俯视读数,导致量取的液体体积偏小,配制溶液的浓度偏低;
C、物品和砝码颠倒,称量的质量变小;
D、俯视读数,导致配制的溶液的体积偏小;
(Ⅱ)(1)根据量筒、滴定管、温度计的构造及准确度进行判断;
(2)根据配制一定物质的量的浓度用到的仪器进行判断;
(3)利用溶解性,Mg(OH)2难溶于水,Ca(OH)2微溶于水,取样品加入蒸馏水溶解,再加少量氯化镁溶液,过滤即可除去杂质,然后根据操作选择合适的仪器即可.
解答 解:(Ⅰ)A、配制一定物质的量浓度的硫酸溶液时,定容摇匀后,发现液面低于刻度线,属于正常情况,不影响配制结果,故A错误;
B、在配制一定物质的量浓度溶液时,用10ml的量筒量取5.0ml液体溶质时俯视读数,俯视读数,导致量取的液体体积减小,配制的溶液浓度偏小,故B错误;
C、用天平称量20.5g某物质,砝码和药品的位置放反,所得药品的质量,药品和砝码颠倒,称量的实际质量偏小,配制的溶液浓度偏小,故C错误;
D、配制一定物质的量浓度溶液时,定容时俯视读数,导致配制的溶液的体积偏小,所得溶液的浓度偏高,故D正确;
故选D.
(Ⅱ)(1)A、①量筒没有0刻度,图中零刻度以下有刻度,应该是温度计,故A错误;
B、②没有零刻度,是量筒,读数是2.5mL,故B错误;
C、③零刻度在上方,是滴定管,读数是2.50mL,故C正确;
D、①是温度计,读数应该是1.5℃,故D错误;
故选ABD;
(2)配制100mL 0.1mol•L-1的氢氧化钠溶液时,还缺少取氢氧化钠固体的药匙和配制溶液的容量瓶,故答案为:药匙和100mL容量瓶;
(3)利用溶解性,Mg(OH)2难溶于水,Ca(OH)2微溶于水,取样品加入蒸馏水溶解,再加适量氯化镁溶液,过滤即可除去杂质;
用到的仪器或用品:a.铁架台(含铁圈、铁夹)、d.烧杯(若干)、e.玻璃棒、f胶头滴管、h.滤纸、i.漏斗.
故答案为:C;取样品加入蒸馏水溶解,再加适量氯化镁溶液,过滤即可除去杂质;a.铁架台(含铁圈、铁夹)、d.烧杯(若干)、e.玻璃棒、f胶头滴管、h.滤纸、i.漏斗.
点评 本题考查了中和滴定的误差分析、仪器选用等知识,注重考查了基础知识和基本操作,本题难度中等.

 名校课堂系列答案
名校课堂系列答案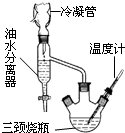 乳酸乙酯(2-羟基丙酸乙酯)常用于调制果香型、乳香型食用和酒用香精.为了在实验室制取乳酸乙酯,某研究性学习小组同学首先查阅资料,获得下列信息:
乳酸乙酯(2-羟基丙酸乙酯)常用于调制果香型、乳香型食用和酒用香精.为了在实验室制取乳酸乙酯,某研究性学习小组同学首先查阅资料,获得下列信息:①部分物质的沸点:
| 物 质 | 水 | 乙醇 | 乳酸 | 苯 | 乳酸乙酯 |
| 沸点/℃ | 100 | 78.4 | 122 | 80.10 | 154 |
该研究性学习小组同学拟采用如图所示(未画全)的主要装置制取乳酸乙酯,其主要实验步骤如下:
第一步:在三颈烧瓶中加入0.1mol无水乳酸、过量的65.0mL无水乙醇、一定量的苯、沸石…;装上油水分离器和冷凝管,缓慢加热回流至反应完全.
第二步:将三颈烧瓶中液体倒入盛有过量某试剂的烧杯中,搅拌并分出有机相后,再用水洗.
第三步:将无水CaCl2加入到水洗后的产品中,过滤、蒸馏.
(1)第一步操作中,还缺少的试剂是浓硫酸;加入苯的目的是形成水、乙醇、苯共沸物,分离反应生成的水,促进酯化反应正向进行;实验过程中,酯化反应进行完全的标志是油水分离器中液体不再增加.
(2)第二步中证明“水洗”已经完成的实验方案是测定水洗液的pH至7.
(3)第三步可以得到较纯净的乳酸乙酯,为获得更纯净的乳酸乙酯,可采用层析法.
(4)利用核磁共振氢谱可以鉴定制备的产物是否为乳酸乙酯,乳酸乙酯分子核磁共振氢谱中有5个峰.
| 选项 | 陈述 | 陈述 |
| A | H2O2、SO2都能使酸性高锰酸钾溶液褪色 | 前者表现出还原性后者表现出漂白性 |
| B | 纯银器表面在空气中渐渐变暗 | 发生化学腐蚀 |
| C | SiO2能与氢氟酸及碱反应 | SiO2是两性氧化物 |
| D | BaSO4饱和溶液中加入饱和Na2CO3 溶液有BaCO3生产 | 说明Kvp(BaSO4)>Kvp(BaSO3) |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
| A. | 熔融状态的Na2O | B. | NaCl晶体 | C. | 液态H2SO4 | D. | 硫酸溶液 |
| A. | 电解精炼铜:阳极质量的减小等于阴极质量的增加 | |
| B. | 氯碱工业:在阴极需要不断加入含有NaOH的蒸馏水 | |
| C. | 合成氨工业:使用催化剂只加快反应速率不影响化学平衡 | |
| D. | 硫酸工业:SO2的转化率高达93.5%~98%,因此接触氧化后的尾气可以直接排放 |
| A. | AgNO3 CuCl2 Cu(NO3)2 | B. | KCl Na2SO4 CuSO4 | ||
| C. | CaCl2 KOH NaNO3 | D. | HCl HNO3 K2SO4 |
| A. | 滴加KI溶液时,KI被氧化,CuI是氧化产物 | |
| B. | 通入SO2后溶液逐渐变成无色,体现了SO2的漂白性 | |
| C. | 通入22.4 L SO2参加反应时,有2NA个电子发生转移 | |
| D. | 上述实验条件下,物质的氧化性:Cu2+>I2>SO2 |