题目内容
11. 乳酸乙酯(2-羟基丙酸乙酯)常用于调制果香型、乳香型食用和酒用香精.为了在实验室制取乳酸乙酯,某研究性学习小组同学首先查阅资料,获得下列信息:
乳酸乙酯(2-羟基丙酸乙酯)常用于调制果香型、乳香型食用和酒用香精.为了在实验室制取乳酸乙酯,某研究性学习小组同学首先查阅资料,获得下列信息:①部分物质的沸点:
| 物 质 | 水 | 乙醇 | 乳酸 | 苯 | 乳酸乙酯 |
| 沸点/℃ | 100 | 78.4 | 122 | 80.10 | 154 |
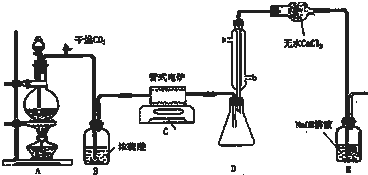
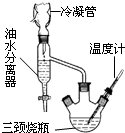
该研究性学习小组同学拟采用如图所示(未画全)的主要装置制取乳酸乙酯,其主要实验步骤如下:
第一步:在三颈烧瓶中加入0.1mol无水乳酸、过量的65.0mL无水乙醇、一定量的苯、沸石…;装上油水分离器和冷凝管,缓慢加热回流至反应完全.
第二步:将三颈烧瓶中液体倒入盛有过量某试剂的烧杯中,搅拌并分出有机相后,再用水洗.
第三步:将无水CaCl2加入到水洗后的产品中,过滤、蒸馏.
(1)第一步操作中,还缺少的试剂是浓硫酸;加入苯的目的是形成水、乙醇、苯共沸物,分离反应生成的水,促进酯化反应正向进行;实验过程中,酯化反应进行完全的标志是油水分离器中液体不再增加.
(2)第二步中证明“水洗”已经完成的实验方案是测定水洗液的pH至7.
(3)第三步可以得到较纯净的乳酸乙酯,为获得更纯净的乳酸乙酯,可采用层析法.
(4)利用核磁共振氢谱可以鉴定制备的产物是否为乳酸乙酯,乳酸乙酯分子核磁共振氢谱中有5个峰.
分析 本题是利用乙醇和乳酸的酯化反应制取乳酸乙酯的实验探究,涉及实验原理酯化反应需要浓硫酸作催化剂,且此反应为可逆反应,可以通过减少生成促进平衡正向移动,还考查了酯化进行完全的标志可通过观察生成物的量不再增加来确实,以及反应后混合物分离提纯,最后还根据乳酸乙酯的结构中等效氢来判断乳酸乙酯分子核磁共振氢谱的特征,
(1)酯化反应过程中需要添加浓硫酸作催化剂和吸水剂,反应混合物中添加苯易于形成共沸物,促进平衡的移动,可根据生成物中油层的量变化来判断反应进行程度;
(2)水洗的目的主要是除去催化作用的硫酸,因此洗涤液显酸性;
(3)利用粗产品中各组分物理化学性质的差异来进行分离;
(4)可先判断乳酸乙酸分子结构中有几种不同环境的氢原子即等效氢,从而确定核磁共振氢谱中有几个峰.
解答 解:(1)酯化反应利用浓硫酸作催化剂和吸水剂,故缺少浓硫酸,酯化反应是可逆反应,混合物中添加苯可形成水、乙醇、苯共沸物,分离反应生成的水,促进酯化反应正向进行,如果收集装置中液体的量不再再增加说明反应已经完全,故答案为:浓硫酸;形成水、乙醇、苯共沸物,分离反应生成的水,促进酯化反应正向进行;油水分离器中液体不再增加;
(2)最后一次洗涤液不显酸性,可说明洗涤完全,因此只要测定一下最后一次水洗液的pH到7即可判断,故答案为:测定水洗液的pH至7;
(3)通过层析进行分离得到更纯净的乳酸乙酯,故答案为:层析;
(4)乳酸乙酯分子的结构简式为CH3CH(OH)COOCH2CH3,分子中有5种不同环境的氢原子,乳酸乙酯分子核磁共振氢谱中有5个峰,故答案为:5.
点评 本题考查酯化反应的原理及混合物的分离与提纯,属基础性考查,难度较低,建议学生重视双基的复习,以不变应万变.

练习册系列答案
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案
相关题目
11.把温度为20℃,浓度为1.0mol•L-1的H2SO4和2.2mol•L-1的碱溶液各50mL混合(溶液密度均为1g•mL-1,比热容为4.184kJ•K-1•kg-1)轻轻搅动,测得酸碱混合液的温度变化数据如下:
则反应NH3•H2O?NH${\;}_{4}^{+}$+OH-的焓变约为(单位:kJ•mol-1)( )
| 反应物 | 起始温度t1℃ | 终止温度t2℃ |
| H2SO4+NaOH | 20 | 33.6 |
| H2SO4+NH3•H2O | 20 | 32.6 |
| A. | 2.1 | B. | 4.2 | ||
| C. | 52.7 | D. | 缺少数据无法计算 |
8.某有机物的结构简式如图此有机物的说法不正确的是( )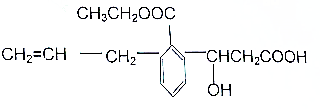

| A. | 可发生的反应类型有:取代、加成、消去、酯化、水解、氧化、中和、聚合 | |
| B. | 1mol该物质与足量NaOH溶液反应,消耗NaOH的物质的量为2mol | |
| C. | 1mol该物质与Na、Na2CO3、NaHCO3反应时,所消耗的物质的量之比为2:1:2,产生的气体在标准状况下的体积比是2:1:2 | |
| D. | 该有机物属于芳香族化合物 |
3. 实验室制备1,2-二溴乙烷的反应原理如下:
实验室制备1,2-二溴乙烷的反应原理如下:
CH3CH2OH→CH2=CH2+H2O
CH2=CH2+Br2→BrCH2CH2Br
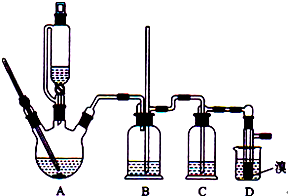
可能存在的副反应有:乙醇在浓硫酸的存在下l40℃脱水生成乙醚.用少量的溴和足量的乙醇制备1,2-二溴乙烷,装置如图所示:有关数据列表如下:
回答下列问题:
(1)在此制备实验中,要尽可能快地把反应温度升高到170℃左右,其目的有ad(填正确选项前的字母)
a.引发反应
b.加快反应速度
c.防止乙醇挥发
d.减少副产物乙醚生成
(2)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在下层(填“上”、“下”)
(3)实验过程中装置B可以防止倒吸,并检查装置C、D是否堵塞,写出装置D堵塞时B中的现象当装置发生堵塞时,B装置中液体会压入的长玻璃导管,甚至溢出导管,以观测和缓解气压增大
(4)判断该制备反应已经结束的最简单方法是溴的颜色完全褪去
(5)反应过程中应用冷水冷却装置D,其主要目的是冷却可避免溴的大量挥发;但又不能过度冷却(如用冰水),其原因是产品1,2-二溴乙烷的熔点(凝固点)低,过度冷却会凝固而堵塞导管.
 实验室制备1,2-二溴乙烷的反应原理如下:
实验室制备1,2-二溴乙烷的反应原理如下:CH3CH2OH→CH2=CH2+H2O
CH2=CH2+Br2→BrCH2CH2Br
可能存在的副反应有:乙醇在浓硫酸的存在下l40℃脱水生成乙醚.用少量的溴和足量的乙醇制备1,2-二溴乙烷,装置如图所示:有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
(1)在此制备实验中,要尽可能快地把反应温度升高到170℃左右,其目的有ad(填正确选项前的字母)
a.引发反应
b.加快反应速度
c.防止乙醇挥发
d.减少副产物乙醚生成
(2)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在下层(填“上”、“下”)
(3)实验过程中装置B可以防止倒吸,并检查装置C、D是否堵塞,写出装置D堵塞时B中的现象当装置发生堵塞时,B装置中液体会压入的长玻璃导管,甚至溢出导管,以观测和缓解气压增大
(4)判断该制备反应已经结束的最简单方法是溴的颜色完全褪去
(5)反应过程中应用冷水冷却装置D,其主要目的是冷却可避免溴的大量挥发;但又不能过度冷却(如用冰水),其原因是产品1,2-二溴乙烷的熔点(凝固点)低,过度冷却会凝固而堵塞导管.