题目内容
3.写出下列离子方程式.(1)钠投入到水中2Na+2H2O=2Na++2OH-+H2↑;
(2)硫酸铵和烧碱两溶液混合并加热NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O;
(3)将氯气通入氢氧化钠溶液制漂白剂和消毒剂Cl2+2OH-=Cl-+ClO-+H2O;
(4)实验室制Cl2MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+H2O;
(5)大理石雕塑上洒上盐酸CaCO3+2H+=Ca2++CO2↑+H2O.
分析 (1)钠与水反应生成氢氧化钠和氢气;
(2)硫酸铵和烧碱两溶液混合并加热反应生成硫酸钠、氨气和水;
(3)氯气与氢氧化钠溶液反应生成氯化钠和次氯酸钠和水;
(4)二氧化锰与浓盐酸在加热条件下发生反应生成氯化锰、氯气和水;
(5)碳酸钙与盐酸反应生成氯化钙和水、二氧化碳.
解答 解:(1)钠与水反应生成氢氧化钠和氢气,离子方程式:2Na+2H2O=2Na++2OH-+H2↑;
故答案为:2Na+2H2O=2Na++2OH-+H2↑;
(2)硫酸铵和烧碱两溶液混合并加热反应生成硫酸钠、氨气和水,离子方程式:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O;
故答案为:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O;
(3)氯气与氢氧化钠溶液反应生成氯化钠和次氯酸钠和水,离子方程式:Cl2+2OH-=Cl-+ClO-+H2O;
故答案为:Cl2+2OH-=Cl-+ClO-+H2O;
(4)二氧化锰与浓盐酸在加热条件下发生反应生成氯化锰、氯气和水,离子方程式:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+H2O;
故答案为:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+H2O;
(5)碳酸钙与盐酸反应生成氯化钙和水、二氧化碳,离子方程式:CaCO3+2H+=Ca2++CO2↑+H2O;
故答案为:CaCO3+2H+=Ca2++CO2↑+H2O.
点评 本题考查了离子方程式的书写,明确反应实质及离子方程式书写方法是解题关键,题目难度不大.

 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案为探讨反应X+Y Z中反应速率与反应物浓度的关系,实验测得X、Y的初始浓度(用c表示,mol/L)与生成物Z的浓度达到0.0042mol/L时所需的时间如右表所示.下列关于该反应反
Z中反应速率与反应物浓度的关系,实验测得X、Y的初始浓度(用c表示,mol/L)与生成物Z的浓度达到0.0042mol/L时所需的时间如右表所示.下列关于该反应反 应速率的判断正确的是( )
应速率的判断正确的是( )
c(X) | c(Y) | 所需时间(秒) |
0.10 | 0.10 | 0.60s |
0.20 | 0.10 | 0.15s |
0.20 | 0.05 | 0.30s |
A.与c(X)成正比且与c(Y)成正比
B.与c(X)成正比且与c(Y)无关
C.与c2(X)成正比且与c(Y)成正比
D.与c2(X)成正比且与c(Y)成反比
| A. | 钠投入水中:Na+H2O═Na++OH-+H2↑ | |
| B. | 碳酸钙溶于醋酸:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| C. | 碳酸氢钙溶液中加入过量的NaOH溶液:Ca2++HCO3-+OH-═CaCO3↓+H2O | |
| D. | 过量的CO2通入Na[Al(OH)4]-溶液中:CO2+[Al(OH)4]-═Al(OH)3↓+HCO3- |
| A. |  | B. | 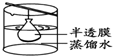 | C. | 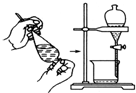 | D. | 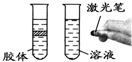 |
| A. | 1:1 | B. | 1:2 | C. | 2:1 | D. | 3:2 |
| A. | 能发生丁达尔效应 | B. | 用FeCl3和烧碱溶液反应制备 | ||
| C. | 微粒直径在1nm-100nm之间 | D. | 能透过滤纸 |
| A. | a:b | B. | $\frac{a}{44}$:$\frac{b}{9}$ | C. | $\frac{a}{12}$:$\frac{b}{12}$ | D. | $\frac{a}{44}$:$\frac{b}{18}$ |
 如图是某学校实验室从化学试剂商店买回的浓硫酸试剂标
如图是某学校实验室从化学试剂商店买回的浓硫酸试剂标