题目内容
13.在一个小烧杯里加入约20g已研磨成粉末的氢氧化钡晶体[Ba(OH)2•8H2O],将小烧杯放在事先已滴有3~4滴水的玻璃片上,然后向烧杯内加入约10g氯化铵晶体,并立即用玻璃棒迅速搅拌.试回答下列问题:(1)写出有关的化学方程式:Ba(OH)2•8H2O+2NH4Cl=BaCl2+2NH3↑+10H2O
(2)观察到“结冰”现象,说明反应是一个吸热(填“放出”或“吸收”)能量的反应,即断开旧化学键吸收(填“放出”或“吸收”)能量>(填“>”或“<”)形成新化学键放出(填“吸收”或“放出”)的能量.
(3)该反应在常温下就可以进行,说明有的吸热反应不需要加热也可以进行.
分析 (1)反应为复分解反应,二者反应生成氨气、水、以及氯化钡;
(2)观察到“结冰”现象,说明该反应为吸热反应;吸热反应中,反应物的总能量小于生成物的总能量,旧键断裂吸收的能量高于新键生成释放的能量;
(3)吸热反应不需要加热也可发生.
解答 解:(1)氯化铵属于铵盐,能和强碱氢氧化钡反应生成氨气、水、以及氯化钡,化学方程式为Ba(OH)2•8H2O+2NH4Cl=BaCl2+2NH3↑+10H2O,
故答案为:Ba(OH)2•8H2O+2NH4Cl═BaCl2+10H2O+2NH3↑;
(2)反应是一个吸热反应,则会观察到“结冰”现象,则反应物的总能量小于生成物的总能量,旧键断裂吸收的能量高于新键生成释放的能量,
故答案为:吸热;吸收;>;放出;
(3)该反应在常温下就可以进行,说明吸热反应不需要加热也可发生,
故答案为:有的吸热反应不需要加热也可发生.
点评 本题考查了化学反应中的能量变化以及吸热反应、放热反应与反应条件的关系,题目难度中等,以Ba(OH)2•8H2O与NH4Cl固体的反应为背景考查了分析问题、解决问题的能力和实验设计能力;反应放出或吸收的热量可以通过触觉感知,也可以通过温度计测量.

练习册系列答案
相关题目
4.下列电离方程式书写错误的是( )
| A. | H2SO4=2H++SO42- | B. | Ba(OH)2=Ba2++2OH- | ||
| C. | Na2CO3=2Na+1+CO3-2 | D. | NaHCO3=Na++HCO3- |
1.有一支25mL酸式滴定管中盛盐酸,液面恰好在amL刻度处,把管内液体放出一部分到bmL刻度线处,盛入量筒内,所得液体体积一定是( )
| A. | (a-b) mL | B. | (25-a)mL | C. | (b-a)mL | D. | 大于a mL |
8.下列化学式能表示一种纯净物的是( )
| A. | C4H10 | B. | C3H6 | C. | C2H6O | D. | CH2Br2 |
5.化学与生活、社会密切相关.下列说法正确的是( )
| A. | 臭氧能对水体消毒,是因为其能杀死水中的病菌 | |
| B. | 执行“限塑令”主要是为了节约资源 | |
| C. | 含磷洗涤剂因为其易被细菌分解,所以不会导致水体污染 | |
| D. | 新装修的住房中放置任何花卉都能降低居室中甲醛的含量 |
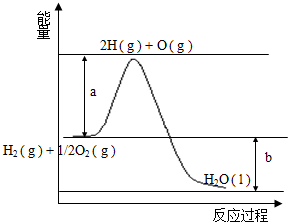 已知H2的燃烧热为285.8kJ•mol-1,反应过程中能量变化如图:请回答下列问题:
已知H2的燃烧热为285.8kJ•mol-1,反应过程中能量变化如图:请回答下列问题: