题目内容
18.下列实验与物质微粒大小无直接关系的是( )| A. |  | B. | 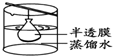 | C. | 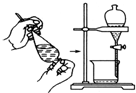 | D. | 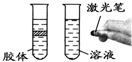 |
分析 浊液、胶体、溶液的本质区别是分散质粒子的大小不同,悬浊液的分散质粒子不能通过滤纸,浊液的分散质粒子不能透过滤纸,胶体、溶液的分散质粒子能透过滤纸;胶体和浊液的分散质粒子不能透过半透膜,溶液的分散质粒子能透过半透膜;
胶体微粒能对光线散射,产生丁达尔效应,而溶液中的离子很小,不能产生丁达尔效应;
萃取利用一种溶质在两种溶剂中的溶解度不同进行分离,与物质微粒大小无直接关系.
解答 解:A.悬浊液的分散质粒子不能通过滤纸,过滤利用了分散质粒子的大小进行分离,故A错误;
B.胶体的分散质粒子不能透过半透膜,溶液的分散质粒子能透过半透膜,渗析利用了分散质粒子的大小进行分离,故B错误;
C.萃取利用一种溶质在两种溶剂中的溶解度不同进行分离,与物质微粒大小无直接关系,故C正确;
D.胶体微粒能对光线散射,产生丁达尔效应,而溶液中的离子很小,不能产生丁达尔效应,丁达尔效应与分散质粒子的大小有关,故D错误;
故选C.
点评 本题考查混合物分离提纯原理及装置,为高频考点,把握混合物分离原理及分离实验为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
9.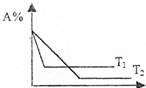 可逆反应A(g)+2B(g)?C(g) 在相同压强时,混和气体中A的百分含量跟反应时间t、温度T的关系如图所示,下列结论正确是( )
可逆反应A(g)+2B(g)?C(g) 在相同压强时,混和气体中A的百分含量跟反应时间t、温度T的关系如图所示,下列结论正确是( )
 可逆反应A(g)+2B(g)?C(g) 在相同压强时,混和气体中A的百分含量跟反应时间t、温度T的关系如图所示,下列结论正确是( )
可逆反应A(g)+2B(g)?C(g) 在相同压强时,混和气体中A的百分含量跟反应时间t、温度T的关系如图所示,下列结论正确是( )| A. | T1>T2,正反应是放热反应 | B. | T1>T2,正反应是吸热反应 | ||
| C. | T2>T1,正反应是放热反应 | D. | T2>T1,正反应是吸热反应 |
10.把V L含有MgS04和K2S04的混合溶液分成5等份,一份加入含a mol NaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含b mol BaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡.则原混合溶液中钾离子的浓度为( )
| A. | $\frac{b-2a}{V}$ | B. | $\frac{2b-5a}{V}$ | C. | $\frac{10b-5a}{V}$ | D. | $\frac{5a-10b}{V}$ |
7.下列离子组一定能够大量共存的是( )
| A. | CO32-Cl- Na+ H+ | B. | K+ Na+ SO42- Ba2+ | ||
| C. | Cl- Na+ Ag+ NO3- | D. | CO32- SO42- Cl- OH- |
8.下列化学式能表示一种纯净物的是( )
| A. | C4H10 | B. | C3H6 | C. | C2H6O | D. | CH2Br2 |
 CH3CH2OH(g)+3H2O(g)需在300℃进行可推测该反应是吸热反应
CH3CH2OH(g)+3H2O(g)需在300℃进行可推测该反应是吸热反应 .
.