题目内容
向5.2g Fe3O4、Fe2O3、Cu的混合物中加入0.5 mol·L?1的硫酸溶液140mL时,固体恰好完全溶解,所得溶液中不含Fe3+,若用过量的CO在高温下还原相同质量的原混合物,固体减少的质量为( )
| A.1.12g | B.6.42g | C.2.24g | D.3.24g |
A
试题分析:在混合物与硫酸混合时发生反应:Fe3O4+4H2SO4=Fe2(SO4)3+FeSO4+4H2O;Fe2O3+3H2SO4= Fe2(SO4)3 +3H2O;Fe2(SO4)3 +Cu= 2FeSO4+ CuSO4。n(Cu)="n{" Fe2(SO4)3}=n(Fe3O4)+n(Fe2O3)向5.2g Fe3O4、Fe2O3、Cu的混合物中加入0.5 mol·L?1的硫酸溶液140mL时,固体恰好完全溶解,所得溶液中不含Fe3+说明溶液为Fe(SO4)2和CuSO4. 用过量的CO在高温下还原相同质量的原混合物,固体减少的质量为其中所含有的氧元素的质量。假设5.2g Fe3O4、Fe2O3、Cu的混合物中Fe3O4、Fe2O3的物质的量分别为X、Y,则Cu的物质的量为(X+Y)。根据题意可得:3X+2Y+X+Y=0.14L×0.5 mol/L=0.07; 232X+160Y+ 64(X+Y)= 5.2.解得X=0.01mol;Y=0.01mol。所以n(O)=4×0.01mol+3×0.01mol=0.07mol. 若用过量的CO在高温下还原相同质量的原混合物,固体减少的质量为m=n·M=0.07mol×16g/mol=1.12g.故选项为A。

练习册系列答案
 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案
相关题目

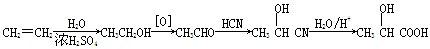
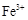 和
和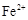 浓度相等。则已反应的
浓度相等。则已反应的