题目内容
8.设NA为阿伏加德罗常数,下列正确的是( )| A. | 1 mol 过氧化钠中阴离子所带的负电荷数为NA | |
| B. | mg${\;}_{Z}^{A}$Xn-中所含电子总数为(Z+n)m$\frac{N_A}{A}$ | |
| C. | 100mL 0.1mol•L-1的稀醋酸中含有H+个数为0.01NA | |
| D. | 11.2L CO2所含的原子个数为1.5NA |
分析 A、过氧化钠中阴离子为O22-;
B、${\;}_{Z}^{A}$Xn-的摩尔质量为Ag/mol,含有(Z+n)个电子;
C、醋酸是弱酸,不能完全电离;
D、二氧化碳所处的状态不明确.
解答 解:A、过氧化钠中阴离子为O22-,而1mol过氧化钠含1mol过氧根,含有的负电荷为2mol即2NA个,故A错误;
B、${\;}_{Z}^{A}$Xn-的摩尔质量为Ag/mol,含有(Z+n)个电子,故mg${\;}_{Z}^{A}$Xn-的物质的量n=$\frac{mg}{Ag/mol}$=$\frac{m}{A}$mol,故含有的电子的物质的量n=$\frac{m}{A}×(Z+n)$mol,即(Z+n)m$\frac{N_A}{A}$个,故B正确;
C、醋酸是弱酸,不能完全电离,故溶液中的氢离子的个数小于0.01NA个,故C错误;
D、二氧化碳所处的状态不明确,故11.2L二氧化碳的物质的量无法计算,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
16.为确定下列置于空气中的物质是否变质,所选检验试剂(括号内物质)不能达到目的是( )
| A. | Na2SO3溶液【Ba(OH)2溶液】 | B. | FeCl2溶液【KSCN溶液】 | ||
| C. | KI【淀粉溶液】 | D. | NaOH溶液【Ba(OH)2溶液】 |
3.下列各项中表达正确的是( )
| A. | 氮气的分子式:N≡N | B. | Na+结构示意图是: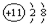 | ||
| C. | 乙醇的结构简式C2H6O | D. | HClO的电子式: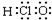 |
13.元素周期表中某区域的一些元素多用于制造半导体材料,它们是( )
| A. | 金属元素和非金属元素分界线附近的元素 | |
| B. | 稀有气体元素 | |
| C. | 左下方区域的金属元素 | |
| D. | 右上方区域的非金属元素 |
20.常温下,下列各组微粒在指定溶液中一定能大量共存的是( )
| A. | 0.1 mol•L-1 Fe(NO3)3溶液中:Mg2+、H+、SO42-、Cl- | |
| B. | 0.1 mol•L-1 KClO溶液中:Na+、H+、Cl-、NO3- | |
| C. | 0.1 mol•L-1氨水中:Ba2+、Ag+、NH4+、NO3- | |
| D. | c(OH-)=10-13 mol•L-1的溶液中:MnO4-、Na+、Br-、CH3CHO |
17.下列性质不属于金属单质通性的是( )
| A. | 一般都容易导电?导热 | B. | 都有金属光泽 | ||
| C. | 都具有较高的熔点 | D. | 一般都有延展性 |
18.下列说法正确的是( )
| A. | HCl气体溶于水时破坏了非极性共价键 | |
| B. | 4.6gNO2溶于水转移0.3mol电子 | |
| C. | 碱金属元素的原子半径越大熔点越低 | |
| D. | 离子化合物和共价化合物在熔融状态下都可以导电 |