题目内容
18.下列说法正确的是( )| A. | HCl气体溶于水时破坏了非极性共价键 | |
| B. | 4.6gNO2溶于水转移0.3mol电子 | |
| C. | 碱金属元素的原子半径越大熔点越低 | |
| D. | 离子化合物和共价化合物在熔融状态下都可以导电 |
分析 A、HCl气体溶于水时破坏了极性共价键;
B、4.6gNO2的物质的量为0.1mol,而1mol的二氧化氮与水反应转移2mol的电子,所以4.6gNO2溶于水转移0.2mol电子;
C、碱金属元素的原子半径越大,金属键越弱;
D、共价化合物在熔融状态下不导电.
解答 解:A、HCl气体溶于水时破坏了极性共价键,故A错误;
B、4.6gNO2的物质的量为0.1mol,而1mol的二氧化氮与水反应转移2mol的电子,所以4.6gNO2溶于水转移0.2mol电子,故B错误;
C、碱金属元素的原子半径越大,金属键越弱,熔点越低,故C正确;
D、共价化合物在熔融状态下不导电,故D错误;
故选C.
点评 本题考查较综合,涉及氧化还原反应中电子的转移、导电性和化学键及物质分类等,为高频考点,注重基础知识的考查,综合性较强,题目难度不大.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
8.设NA为阿伏加德罗常数,下列正确的是( )
| A. | 1 mol 过氧化钠中阴离子所带的负电荷数为NA | |
| B. | mg${\;}_{Z}^{A}$Xn-中所含电子总数为(Z+n)m$\frac{N_A}{A}$ | |
| C. | 100mL 0.1mol•L-1的稀醋酸中含有H+个数为0.01NA | |
| D. | 11.2L CO2所含的原子个数为1.5NA |
9.氯气是一种重要的工业原料.工业上利用反应在3Cl2+2NH3═N2+6HCl检查氯气管道是否漏气.下列说法错误的是( )
| A. | 该反应中氨气是还原剂 | B. | 该反应利用了Cl2的强氧化性 | ||
| C. | 该反应HCl是氧化产物 | D. | 生成1molN2有6mol电子转移 |
6.如表是元素周期的一部分,出了七种元素的周期表中的位置:
请用化学符号按要求回答下列问题:
(1)这七种元素中,非金属性最强的是F,在元素周期表中的位置第二周期ⅦA族
(2)元素①与②形成摩尔质量为44g/mol的物质,它的电子式是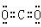
(3)③、⑥、⑦三种元素的原子半径由大到小的顺序是Al>Cl>F.
(4)④元素最高价氧化物对应的水化物与⑥元素的最高价氧化物对应的水化物反应的化学反应方程式是NaOH+Al(OH)3=NaAlO2+2H2O
(5)④、⑤、⑥三种元素最高价氧化物的水化物碱性强弱顺序是NaOH>Mg(OH)2>Al(OH)3.
| 主族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 2 | ① | ② | ③ | ||||
| 3 | ④ | ⑤ | ⑥ | ⑦ |
(1)这七种元素中,非金属性最强的是F,在元素周期表中的位置第二周期ⅦA族
(2)元素①与②形成摩尔质量为44g/mol的物质,它的电子式是
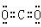
(3)③、⑥、⑦三种元素的原子半径由大到小的顺序是Al>Cl>F.
(4)④元素最高价氧化物对应的水化物与⑥元素的最高价氧化物对应的水化物反应的化学反应方程式是NaOH+Al(OH)3=NaAlO2+2H2O
(5)④、⑤、⑥三种元素最高价氧化物的水化物碱性强弱顺序是NaOH>Mg(OH)2>Al(OH)3.
13.化学反应速率最主要取决于( )
| A. | 是否使用催化剂 | B. | 反应物的性质 | C. | 反应的温度 | D. | 反应的压强 |
3.下列说法错误的是( )
| A. | 分子式分别为C2H4和C4H8的两种有机物一定是同系物 | |
| B. | 同一种分子式可能代表不止一种物质 | |
| C. | 苯的产量是石化工业发展水平的标志 | |
| D. | 烷烃的通式是:CnH2n+2 |
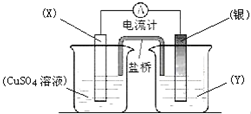 依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示.
依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示.