题目内容
【题目】某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
①将碱式滴定管用蒸馏水洗净后,用待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于“0”刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放出25.00mL待测溶液到锥形瓶中。
②将酸式滴定管用蒸馏水洗净后,立即向其中注入0.1000mol·L-1标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于“0”刻度以下的位置,记下读数。
③向锥形瓶中滴入酚酞作指示剂,进行滴定。滴定至终点,测得所耗盐酸的体积为V1mL。
④重复以上过程,但在滴定过程中向锥形瓶中加入5mL的蒸馏水,测得所耗盐酸的体积为V2mL。试回答下列问题:
(1)滴定终点时的现象为锥形瓶中的溶液由______;
(2)滴定时边滴边摇动锥形瓶,眼睛应观察_______;
(3)该小组在步骤①中的错误是______,由此造成的测定结果________(填“偏高”或“偏低”或“无影响”);
(4)步骤②缺少的操作是_____;
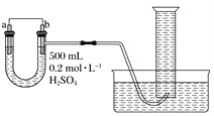
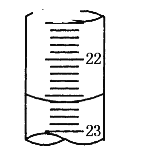
(5)如上图是某次滴定时的滴定管中的液面,其读数为___mL;
(6)根据下列数据:
测定次数 | 待测液体积/mL | 标准盐酸体积/mL | |
滴定前读数/mL | 滴定后读数/mL | ||
第一次 | 25.00 | 0.40 | 20.38 |
第二次 | 25.00 | 4.00 | 24.02 |
请计算待测烧碱溶液的物质的量浓度。(请写出解答过程)_______________
【答案】浅红色变为无色,且半分钟之内不褪色 锥形瓶中溶液颜色变化 待测溶液润洗锥形瓶 偏高 用标准液润洗滴定管2~3次 22.60 0.0800mol/L
【解析】
(1)根据滴定终点,锥形瓶中的溶液从浅红色变为无色时,且半分钟内不褪色,应停止滴定;
(2)根据滴定操作分析;
(3)根据待测溶液润洗锥形瓶,会使的待测液的物质的量增多;根据c(待测)=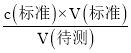
分析误差;
(4)根据酸式滴定管用蒸馏水洗净后,应用标准液润洗;
(5)结合滴定管0刻度在上判断溶液体积读数;
(6)根据c(待测)=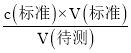 计算,V(标准)用两次的平均值。
计算,V(标准)用两次的平均值。
(1)用标准盐酸溶液滴定未知浓度的NaOH溶液,使用酚酞为指示剂,开始时溶液为碱性,因此溶液显红色,当达到滴定终点时,锥形瓶中的溶液从浅红色变为无色时,且半分钟内不褪色,停止滴定;
(2)中和滴定时,左手控制滴定管的活塞,右手摇动锥形瓶,眼睛注视锥形瓶中溶液颜色变化。当锥形瓶中的溶液从浅红色变为无色时,且半分钟内不褪色,停止滴定;
(3)根据待测溶液润洗锥形瓶,会使的待测液的物质的量增多,造成V(标准)偏大,根据c(待测)=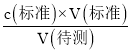 ,可知c(标准)偏高;
,可知c(标准)偏高;
(4)根据酸式滴定管用蒸馏水洗净后,应用标准液润洗滴定管2~3次;
(5)滴定管0刻度在上,大刻度在下的结构,根据滴定管中液体凹液面的位置可确定该溶液体积读数为22.60mL;
(6)V(标准)═[(20.38-0.40)+(24.02-4.00)]mL÷2═20.00mL,c(待测)= ═0.0800mol/L。
═0.0800mol/L。

【题目】下列各组物质,不能按如图(“→”表示反应一步完成)关系转化的是

选 项 | a | b | c |
A | Al2O3 | NaAlO2 | Al(OH)3 |
B | Al | Al(OH)3 | Al2O3 |
C | AlCl3 | Al(OH)3 | NaAlO2 |
D | MgCl2 | Mg(OH)2 | MgO |
A. AB. BC. CD. D