题目内容
【题目】硫酸镁在医疗上具有镇静、抗挛等功效。以菱镁矿(主要成分是MgCO3)为主要原料制备硫酸镁的方法如下:
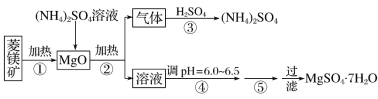
(1)步骤②中发生反应的离子方程式为__________________________________________。
(2)步骤④中调节pH=6.0~6.5的目的是_______________________________________。
(3)步骤⑤的操作为________________________________________________________。
(4)若要除去MgSO4溶液中的FeSO4应先加________,再加入过量__________,过滤即可把杂质除尽;请用离子方程式以及文字说明除杂原理___________________________________
(5)已知酸碱指示剂百里酚蓝变色的pH范围如表所示:
pH | <8.0 | 8.0~9.6 | >9.6 |
颜色 | 黄色 | 绿色 | 蓝色 |
25 ℃时,向Mg(OH)2的饱和溶液中滴加2滴百里酚蓝指示剂,溶液所呈现的颜色为____________(已知25 ℃时 ,Ksp[Mg(OH)2]=5.6×10-12 )。
【答案】2NH4++MgO==Mg2++2NH3↑+H2O 抑制Mg2+水解,以便得到较纯的产品 蒸发浓缩、冷却结晶 过氧化氢 镁粉(或 氧化镁 或碳酸镁或氢氧化镁) 利用 Fe3++3H2O ![]() Fe(OH)3+3H+ , 加入镁粉(或 氧化镁 或碳酸镁或氢氧化镁)消耗 Fe3+水解出的H+,促使平衡右移,使Fe3+为转化Fe(OH)3而除去 蓝色
Fe(OH)3+3H+ , 加入镁粉(或 氧化镁 或碳酸镁或氢氧化镁)消耗 Fe3+水解出的H+,促使平衡右移,使Fe3+为转化Fe(OH)3而除去 蓝色
【解析】
(1)步骤②中发生反应的为硫酸铵和氧化镁反应生成氨气、硫酸镁和水;
(2)步骤④中将硫酸镁溶液蒸发、结晶时,调节pH为弱酸性,抑制镁离子的水解;
(3)根据温度较高时会导致MgSO4![]() 7H2O中的结晶水失去分析操作方法;
7H2O中的结晶水失去分析操作方法;
(4) 若要除去MgSO4溶液中的FeSO4应先加过氧化氢,将Fe2+氧化为Fe3+,再加入过量镁粉(或 氧化镁 或碳酸镁或氢氧化镁),利用 Fe3++3H2O ![]() Fe(OH)3+3H+ , 加入镁粉(或 氧化镁 或碳酸镁或氢氧化镁)消耗 Fe3+水解出的H+,促使平衡右移,使Fe3+为转化Fe(OH)3而除去;
Fe(OH)3+3H+ , 加入镁粉(或 氧化镁 或碳酸镁或氢氧化镁)消耗 Fe3+水解出的H+,促使平衡右移,使Fe3+为转化Fe(OH)3而除去;
(5) Mg(OH)2的饱和溶液中的溶度积计算饱和溶液中的氢氧根离子浓度,结合水溶液中离子积计算氢离子浓度计算pH,然后结合表中数据判断溶液所呈现的颜色。
(1)步骤②中发生反应的为硫酸铵和氧化镁反应生成氨气、硫酸镁和水,反应的离子方程式为2NH4++MgO![]() Mg2++2NH3↑+H2O,
Mg2++2NH3↑+H2O,
因此,本题正确答案是:2NH4++MgO![]() Mg2++2NH3↑+H2O;
Mg2++2NH3↑+H2O;
(2)步骤④中将硫酸镁溶液蒸发、结晶时,为了抑制镁离子的水解,调节pH为弱酸性,使镁离子的水解平衡逆向移动,得到纯净的硫酸镁晶体,
因此,本题正确答案是:抑制Mg2+水解,以便得到较纯的产品;
(3) MgSO4![]() 7H2O在加热条件下容易失去结晶水,无法得到纯净的MgSO4
7H2O在加热条件下容易失去结晶水,无法得到纯净的MgSO4![]() 7H2O,所以从硫酸镁溶液中获得MgSO4
7H2O,所以从硫酸镁溶液中获得MgSO4![]() 7H2O的方法为蒸发浓缩、冷却结晶,
7H2O的方法为蒸发浓缩、冷却结晶,
因此,本题正确答案是:蒸发浓缩、冷却结晶;
(4) 若要除去MgSO4溶液中的FeSO4应先加过氧化氢,将Fe2+氧化为Fe3+,再加入过量镁粉(或 氧化镁 或碳酸镁或氢氧化镁),利用 Fe3++3H2O ![]() Fe(OH)3+3H+ , 加入镁粉(或 氧化镁 或碳酸镁或氢氧化镁)消耗 Fe3+水解出的H+,促使平衡右移,使Fe3+为转化Fe(OH)3而除去;
Fe(OH)3+3H+ , 加入镁粉(或 氧化镁 或碳酸镁或氢氧化镁)消耗 Fe3+水解出的H+,促使平衡右移,使Fe3+为转化Fe(OH)3而除去;
因此,本题正确答案是:过氧化氢;镁粉(或 氧化镁 或碳酸镁或氢氧化镁);利用 Fe3++3H2O ![]() Fe(OH)3+3H+ , 加入镁粉(或 氧化镁 或碳酸镁或氢氧化镁)消耗 Fe3+水解出的H+,促使平衡右移,使Fe3+为转化Fe(OH)3而除去;
Fe(OH)3+3H+ , 加入镁粉(或 氧化镁 或碳酸镁或氢氧化镁)消耗 Fe3+水解出的H+,促使平衡右移,使Fe3+为转化Fe(OH)3而除去;
(5)25 ℃时,Mg(OH)2的溶度积Ksp=5.6×10-12,根据反应Mg(OH)2(s)Mg2+(aq)+2OH-(aq)可得:c(Mg2+)c2(OH-)=5.6×10-12,
设c(OH-)=2 c(Mg2+)=x,则:0.5x![]() x2=5.6×10-12,
x2=5.6×10-12,
计算得出:x=2.24![]() 10-4mol/L,c(H+)=
10-4mol/L,c(H+)=![]() mol/L=4.5
mol/L=4.5![]() 10-11mol/L,
10-11mol/L,
溶液的pH=10.4>9.6,所以溶液呈蓝色,
因此,本题正确答案是:蓝色。

 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案【题目】I-可以作为水溶液中SO2歧化反应的催化剂,可能的催化过程如下。i.SO2+4I-+4H+![]() S↓+2I2+2H2O ii.I2+2H2O+SO2
S↓+2I2+2H2O ii.I2+2H2O+SO2![]() SO42- +4H++2I-
SO42- +4H++2I-
探究i、ii反应速率与SO2歧化反应速率的关系,实验如下:分别将18 mL SO2饱和溶液加入到2 mL下列试剂中,密闭放置观察现象。(已知:I2易溶解在KI溶液中)
序号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
试剂组成 | 0.4 mol·L-1 KI | a mol·L-1 KI 0.2 mol·L-1 H2SO4 | 0.2 mol·L-1 H2SO4 | 0.2 mol·L-1 KI 0.0002 mol I2 |
实验现象 | 溶液变黄,一段时间后出现浑浊 | 溶液变黄,出现浑浊较A快 | 无明显现象 | 溶液由棕褐色很快褪色,变成黄色,出现浑浊较A快 |
下列说法不正确的是( )
A. 水溶液中SO2歧化反应方程式为3SO2+2H2O ![]() 2H2SO4 +S↓
2H2SO4 +S↓
B. II是I的对比实验,则a=0.4
C. 比较I、II、III,可得出的结论是:I是SO2歧化反应的催化剂,H+单独存在时不具有催化作用,但H+可以加快歧化反应速率
D. 实验表明,SO2的歧化反应速率IV>I,原因是反应i比ii快;IV中由反应ii产生的H+使反应i加快