题目内容
【题目】加碘食盐中加入的碘酸钾是一种白色结晶粉末,常温下很稳定,加热至560℃开始分解,在酸性条件下碘酸钾是一种较强的氧化剂,可与碘化物、亚硫酸盐等还原性物质反应。工业生产碘酸钾的流程如下:
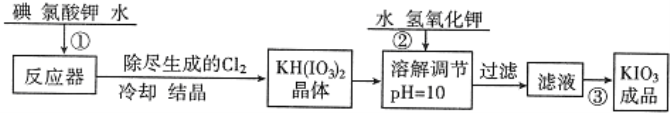
(1)已知步骤①反应器中发生的反应中,单质碘和氯酸钾的物质的量之比为6:11,反应器中发生的化学方程式为6I2+11KClO3+3H2O→6KH(IO3)2+5KCl+3Cl2↑。参照碘酸钾的溶解度:
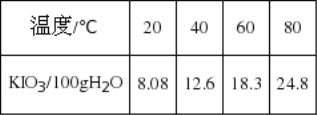
操作③得到碘酸钾晶体,方法是____________、____________:
(2)已知: KIO3+ 5KI+3H2SO4=3K2SO4+3I2+3H2O;I2+2S2O32—=2I—+S4O62—
检验加碘食盐中的碘元素,学生甲利用碘酸钾与碘化钾在酸性条件下发生反应。用四氯化碳检验碘单质时,看到的明显现象有____________
(3)检验加碘食盐中碘的含量,学生乙设计的实验步骤如下:
①准确称取wg食盐,加适量蒸馏水使其完全溶解;
②用稀硫酸酸化所得食盐溶液,加入过量KI溶液充分混合;
③以淀粉为指示剂,逐滴加入2.0╳10—3mol/L的Na2S2O310.0mL,恰好反应完全。
则加碘食盐样品中的碘元素含量是_____ mg/kg (以含w 的代数式表示)。
(4)学生丙又对纯净的NaCl进行了下列实验:

请推测实验中产生蓝色现象的可能原因____________,用化学方程式表示。
(5)根据学生丙的实验结果,学生乙测得的食盐中碘元素的含量可能____________ (填“偏高”、“偏低"或“准确")。原因是____________
【答案】蒸发浓缩 降温结晶 下层四氯化碳呈紫色 ![]() 4 I—+4H+ +O2=2 I2+2H2O 偏高 过量的I—会被空气中的氧气氧化为I2
4 I—+4H+ +O2=2 I2+2H2O 偏高 过量的I—会被空气中的氧气氧化为I2
【解析】
(1)由KIO3溶液得到KIO3成品,则需要将溶剂蒸发掉,而得到浓缩的KIO3溶液,该操作为蒸发浓缩;为了防止形成的晶体KIO3受热分解,应停止加热,用仪器的余热蒸干溶剂,该操作叫作降温结晶;
(2)由于碘单质易溶于四氯化碳,所以用四氯化碳检验碘单质时,混合液分层,下层为四氯化碳层,由于萃取了碘单质,下层液体的颜色为紫红色;故答案为:液体分层,下层液体呈现紫红色;
(3)设碘酸钾的物质的量为x,根据反应KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O、I2+2S2O32-=2I-+S4O62-可得关系式:KIO3~3I2~6S2O32-,
则 KIO3~3I2~6S2O32-
1 6
x 2.0×10-3mol/L×0.01L
x=![]() =
=![]() ×10-5mol,根据碘原子守恒知,碘元素的质量=
×10-5mol,根据碘原子守恒知,碘元素的质量=![]() ×10-5mol×127g/mol=
×10-5mol×127g/mol=![]() ×10-5molg,所以碘元素的质量分数为:
×10-5molg,所以碘元素的质量分数为:![]() ×100%=
×100%=
![]() mg/kg,故答案为:
mg/kg,故答案为:![]() ;
;
(4)酸性条件下,碘离子被氧气氧化生成碘单质,离子反应方程式为:4I-+4H++O2=2I2+2H2O;且酸性条件下,过量的碘离子易被空气中氧气氧化生成碘单质,导致测定结果偏大,故答案为:4I-+4H++O2→2I2+2H2O;学生乙实验结果会偏大;过量的I-会被空气中的氧气氧化为I2。

 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案【题目】硫酸镁在医疗上具有镇静、抗挛等功效。以菱镁矿(主要成分是MgCO3)为主要原料制备硫酸镁的方法如下:
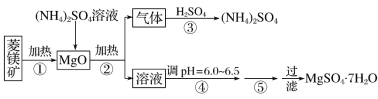
(1)步骤②中发生反应的离子方程式为__________________________________________。
(2)步骤④中调节pH=6.0~6.5的目的是_______________________________________。
(3)步骤⑤的操作为________________________________________________________。
(4)若要除去MgSO4溶液中的FeSO4应先加________,再加入过量__________,过滤即可把杂质除尽;请用离子方程式以及文字说明除杂原理___________________________________
(5)已知酸碱指示剂百里酚蓝变色的pH范围如表所示:
pH | <8.0 | 8.0~9.6 | >9.6 |
颜色 | 黄色 | 绿色 | 蓝色 |
25 ℃时,向Mg(OH)2的饱和溶液中滴加2滴百里酚蓝指示剂,溶液所呈现的颜色为____________(已知25 ℃时 ,Ksp[Mg(OH)2]=5.6×10-12 )。
