题目内容
【题目】已知A、B、C、D、E、F、G都是元素周期表中短周期主族元素,它们的原子序数依次增大。A是周期表中原子半径最小的元素,D3B中阴、阳离子具有相同的电子层结构,B、C均可分别与A形成10个电子分子,B、C属同一周期,两者可以形成许多种共价化合物,C、F属同一主族,B原子最外电子层的p能级上的电子处于半满状态,C的最外层电子数是内层电子数的3倍,E最外层电子数比最内层多1。请用具体的元素回答下列问题:
(1)E元素原子基态电子排布式____________。
(2)用电子排布图表示F元素原子的价电子排布图________________。
(3)F、G元素对应的最高价含氧酸中酸性较强的分子式为_____________________。
(4)离子半径D+______B3-,第一电离能B______C,电负性C______F(填“<”、“>”或“=”)。
(5)A、C形成的两种常见分子电子式_____________;_____________(其中一种为绿色氧化剂)常见阴离子电子式为______________________。
(6)写出E与D的最高价氧化物对应的水化物反应的化学方程式______________。
【答案】1s22s22p63s23p1 ![]() HClO4 < > >
HClO4 < > > 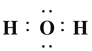
![]()
![]() 2Al+2NaOH+2H2O=2NaAlO2+3H2↑
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
【解析】
A、B、C、D、E、F、G都是元素周期表中短周期主族元素,它们的原子序数依次增大,A是周期表中原子半径最小的元素,则A是H元素,D3B中阴、阳离子具有相同的电子层结构,B原子最外电子层的p能级上的电子处于半满状态,为第VIA族元素,B为-3价、D为+1价且D是金属元素,D的原子序数大于B、C,则D为Na元素、B为N元素,B、C均可分别与A形成10个电子分子,B、C属同一周期,两者可以形成许多种共价化合物,C的最外层电子数是内层电子数的3倍,则C是O元素,C、F属同一主族,则F是S元素,E最外层电子数比最内层多1,则E最外层电子数为3,E是Al元素,G的原子序数大于F,且为短周期主族元素,则G是Cl元素,
(1)通过以上分析知,E是Al元素,其原子核外有13个电子,根据构造原理知其基态原子核外电子排布式为1s22s22p63s23p1;
(2)F为S元素,其价电子为3s、3p电子,其价电子排布图为![]() ;
;
(3)元素的非金属性越强,其最高价氧化物的水化物酸性越强,Cl元素的非金属性大于S元素,则F、G元素对应的最高价含氧酸中酸性较强的分子式为HClO4;
(4)电子层结构相同的离子,离子半径随着原子序数的增大而减小,所以离子半径D+<B3-,
C是O元素、F是S元素,同一主族元素中,电负性随着原子序数的增大而减小,所以电负性C>F;
(5)A、C形成的两种常见分子为水分子和过氧化氢分子,其电子式分别为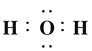 、
、![]() ;常见阴离子氢氧根离子的电子式为
;常见阴离子氢氧根离子的电子式为![]() ;
;
(6)D的最高价氧化物的水化物是NaOH,铝和氢氧化钠溶液反应生成偏铝酸钠和氢气,反应方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑。

 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案【题目】硫酸镁在医疗上具有镇静、抗挛等功效。以菱镁矿(主要成分是MgCO3)为主要原料制备硫酸镁的方法如下:
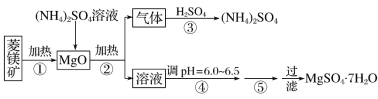
(1)步骤②中发生反应的离子方程式为__________________________________________。
(2)步骤④中调节pH=6.0~6.5的目的是_______________________________________。
(3)步骤⑤的操作为________________________________________________________。
(4)若要除去MgSO4溶液中的FeSO4应先加________,再加入过量__________,过滤即可把杂质除尽;请用离子方程式以及文字说明除杂原理___________________________________
(5)已知酸碱指示剂百里酚蓝变色的pH范围如表所示:
pH | <8.0 | 8.0~9.6 | >9.6 |
颜色 | 黄色 | 绿色 | 蓝色 |
25 ℃时,向Mg(OH)2的饱和溶液中滴加2滴百里酚蓝指示剂,溶液所呈现的颜色为____________(已知25 ℃时 ,Ksp[Mg(OH)2]=5.6×10-12 )。