题目内容
【题目】甲醇是人们开发和利用的一种新能源。已知:
①2H2(g)+O2(g)=2H2O(l) △H1=-571.8kJ· mol-1
②CH3OH(g)+![]() O2(g)=CO2(g)+2H2(g) △H=-192.9 kJ· mol-1
O2(g)=CO2(g)+2H2(g) △H=-192.9 kJ· mol-1
(1)甲醇蒸汽完全燃烧的热化学方程式为_____________。
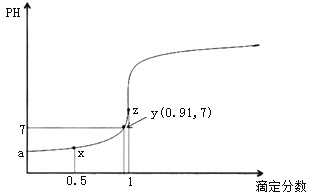
(2)反应②中的能量变化如下图所示,则△H2=______(用E1和E2表示)。

(3)H2(g)的燃烧热为__________ kJ· mol-1。
(4)请你分析H2(g)作为能源比甲醇蒸汽作为能源的优点:__________________(写出一点)
【答案】CH3OH(g)+![]() O2(g)═CO2(g)+2H2O(l)△H2=-764.7kJ/mol; E1-E2 285.9 来源广、热值高、不污染环境
O2(g)═CO2(g)+2H2O(l)△H2=-764.7kJ/mol; E1-E2 285.9 来源广、热值高、不污染环境
【解析】
(1)依据热化学方程式和盖斯定律计算得到所需热化学方程式;
(2)依据反应焓变△H=生成物总能量-反应物总能量分析;
(3)依据燃烧热的概念是1mol可燃物完全燃烧生成稳定氧化物放出的热量,结合热化学方程式分析计算;
(4)根据氢能源的优点和氢能源的开发和利用的最新动向即可作答。
(1)①2H2(g)+O2(g)=2H2O(l) △H1=-571.8kJ· mol-1
②CH3OH(g)+![]() O2(g)=CO2(g)+2H2(g) △H=-192.9 kJ· mol-1
O2(g)=CO2(g)+2H2(g) △H=-192.9 kJ· mol-1
由盖斯定律②+①得到甲醇蒸气完全燃烧的热化学反应方程式为:CH3OH(g)+![]() O2(g)═CO2(g)+2H2O(l)△H2=-764.7kJ/mol;
O2(g)═CO2(g)+2H2O(l)△H2=-764.7kJ/mol;
(2)反应②中的能量变化如图所示,依据图象分析,反应焓变△H=生成物总能量-反应物总能量,△H2=E1-E2;
(3)燃烧热的概念是1mol可燃物完全燃烧生成稳定氧化物放出的热量,根据2H2(g)+O2(g)═2H2O(l) △H1=-571.8kJ/mol可知2mol氢气完全燃烧生成液态水放出的热量为571.8kJ,则1mol氢气完全燃烧生成液态水放出的热量为285.9kJ,故氢气燃烧热为285.9kJ/mol;
(4)地球上水资源丰富,可以从水中提取氢气,说明资源广泛;依据燃烧热计算分析,氢气的燃烧值高;因为氢气燃烧产物是水,不污染环境。

【题目】氨氧化法制硝酸的主要反应是:4NH3(g) + 5O2(g) ![]() 4NO(g) + 6H2O(g)。
4NO(g) + 6H2O(g)。
(1)升高温度,反应的平衡常数K值减小,则该反应的焓变△H_____0(填“>”、“<”或“=”)。
(2)下列能说明上述反应已达到平衡状态__________(填序号)
A.NH3的浓度不随时间变化
B.v正(O2)= v逆(NO)
C.体系的分子总数不再变化
D.单位时间内消耗4molNH3的同时生成6molH2O
(3)若其他条件不变,下列关系图错误的是______(选填序号)。
A.  B.
B.  C.
C.  D.
D. 
(4)在容积固定的密闭容器中发生上述反应,容器内各物质的浓度如下表:
时间/浓度/(mol·L-1) | c(NH3) | c(O2) | c(NO) | c(H2O) |
起始 | 4.0 | 5.5 | 0 | 0 |
第 2 min | 3.2 | 0.8 | 1.2 | |
第 4 min | 2.0 | 3.0 | 2.0 | 3.0 |
第 6 min | 2.0 | 3.0 | 2.0 | 3.0 |
①上表中空白处应填的数字为______。
②反应在第 2 min 到第 4 min 时,反应速率v(O2)=___________。
③反应在第 2 min 时改变了条件,改变的条件可能______;该条件下,反应的平衡常数K=_______(只写计算结果,不标单位)。