题目内容
【题目】甲醛是一种重要的化工原料,常用于生产脲醛树脂及酚醛树脂,在木材加工中的地位及其重要。
(1)工业中甲醛的制备方法常用以下几种。
①甲醇氧化法
CH3OH(g)=HCHO(g)+H2(g) △H = +84kJ/mol
2H2(g)+O2(g)=2H2O(g) △H = -484kJ/mol
CH3OH(g)与O2(g)反应生成HCHO(g)和H2O(g)的热化学方程式是_______。
②天然气氧化法
在600-680℃下,使天然气(主要成分是CH4)和空气的混合物通过铁、钼等的氧化物催化剂,直接氧化生成甲醛。反应的化学方程式是_______。
(2)甲醛是污染室内环境的主要污染物,被称为室内污染“第一杀手”。
①去除甲醛有多种方法,其中,催化氧化法是一种比较高效的除甲醛方法。Na-Pt/TiO2催化剂催化氧化甲醛的反应机理如下图所示:
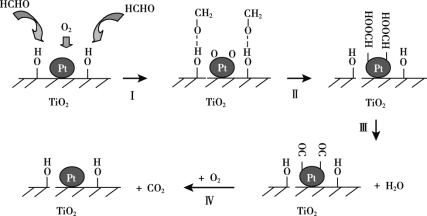
下列有关说法正确的是______(选填字母序号)。
a.该方法除去甲醛的化学方程式是:HCHO+O2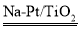 CO2+H2O
CO2+H2O
b.Na-Pt/TiO2催化剂能加快甲醛氧化速率,也能提高甲醛的转化率
c.反应过程中,HCHO只有部分化学键发生断裂
② 为测定居室中甲醛含量,将50L居室中气体缓缓通入25.00mL 0.01molL-1高锰酸钾酸性溶液中,使空气中的甲醛完全吸收,再用0.05molL-1H2C2O4溶液滴定,至终点时消耗H2C2O4溶液12.20mL 。
反应原理为:4MnO4—+12H++5HCHO=4Mn2++5CO2↑+11H2O
2MnO4— +6H++5H2C2O4=2Mn2++10CO2↑+8H2O
滴定终点的现象是_______。该室内空气中甲醛的含量是______mg/L。
【答案】2CH3OH(g)+O2(g)=2HCHO(g)+2H2O(g) △H = -316kJ/mol CH4+O2 = HCHO+H2O a c 高锰酸钾紫色褪去 0.0045mg/L
【解析】
(1)根据盖斯定律进行分析计算;
②CH4和空气的混合物通过铁、钼等的氧化物催化剂,生成甲醛,根据电子守恒和元素守恒分析可知还生成水;
(2)①a.由图可知生成二氧化碳和水;
b.催化剂对平衡移动无影响;
c.图中C=O未断裂;
②高锰酸钾为紫色,结合4MnO4-+12H++5HCHO═4Mn2++5CO2↑+11H2O、2MnO4-+6H++5H2C2O4═2Mn2++10CO2↑+8H2O计算。
:(1)①由I.CH3OH(g)═HCHO(g)+H2(g)△H=+84kJ/mol
II.2H2(g)+O2(g)═2H2O(g)△H=-484kJ/mol
结合盖斯定律可知,I×2+II得到2CH3OH(g)+O2(g)═2HCHO(g)+2H2O(g)△H=-316kJ/mol,
故答案为:2CH3OH(g)+O2(g)═2HCHO(g)+2H2O(g)△H=-316kJ/mol;
②CH4和空气的混合物通过铁、钼等的氧化物催化剂,直接氧化生成甲醛,根据电子守恒和元素守恒分析可知还生成水,反应为CH4+O2![]() HCHO+H2O,故答案为:CH4+O2
HCHO+H2O,故答案为:CH4+O2![]() HCHO+H2O;
HCHO+H2O;
(2)①a.由图可知生成二氧化碳和水,除去甲醛的化学方程式是:HCHO+O2 ═CO2+H2O,故正确;
b.催化剂对平衡移动无影响,可加快反应速率,甲醛的转化率不变,故错误;
c.图中C=O未断裂,则反应过程中,HCHO只有部分化学键发生断裂,故正确;
故答案为:ac;
②滴定终点的现象是高锰酸钾紫色褪去,且半分钟不变,由2MnO4-+6H++5H2C2O4═2Mn2++10CO2↑+8H2O可知,剩余的高锰酸钾为0.0122L×0.05molL-1×![]() =0.000244mol,则由4MnO4-+12H++5HCHO═4Mn2++5CO2↑+11H2O可知,HCHO的物质的量为(0.025L×0.01mol/L-0.000244mol)×
=0.000244mol,则由4MnO4-+12H++5HCHO═4Mn2++5CO2↑+11H2O可知,HCHO的物质的量为(0.025L×0.01mol/L-0.000244mol)×![]() =0.0000075mol,该室内空气中甲醛的含量是
=0.0000075mol,该室内空气中甲醛的含量是![]() =0.0045mg/L,
=0.0045mg/L,
故答案为:高锰酸钾紫色褪去;0.0045。

 特高级教师点拨系列答案
特高级教师点拨系列答案【题目】常温下,浓度均为![]() 的4种钠盐溶液pH如下:下列说法不正确的是( )
的4种钠盐溶液pH如下:下列说法不正确的是( )
溶质 |
|
| NaClO |
|
pH |
|
|
|
|
A.四种溶液中,![]() 溶液中水的电离程度最大
溶液中水的电离程度最大
B.![]() 溶液显酸性的原因是:
溶液显酸性的原因是:![]()
C.向氯水中加入少量![]() ,可以增大氯水中次氯酸的浓度
,可以增大氯水中次氯酸的浓度
D.常温下,相同物质的量浓度的![]() 、
、![]() 、HClO,pH最小的是
、HClO,pH最小的是![]()
【题目】已知H2O2分解速率受多种因素影响,某小组对此进行探究,得到如下结果。下列说法不正确的是
序号 | H2O2体积(ml) | FeCl3体积(ml) | 混合溶液pH | 纯H2O2pH | 分解完全时间(s) |
1 | 20 | 10 | 1.00 | 2.92 | 几乎不分解 |
2 | 20 | 10 | 2.92 | 2.92 | 202 |
3 | 20 | 10 | 7.50 | 2.92 | 192 |
4 | 20 | 10 | 9.50 | 2.92 | 139 |
5 | 20 | 10 | 10.50 | 2.92 | 77 |
表1 (200C) | |||||
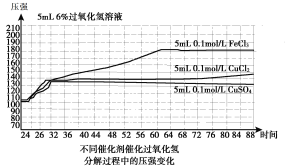
图1(200C)
A.表1表明,其他条件相同时,碱性条件下H2O2分解速率快于酸性条件下
B.图1表明,其他条件相同时,铜盐对H2O2分解的催化效果好于铁盐
C.图1表明,其他条件相同时,CuCl2对H2O2分解的催化效果好于CuSO4
D.以上实验表明,催化剂、溶液酸碱性对H2O2分解速率都有影响
【题目】有a、b、c、d四个金属电极,G为电流计。有关的反应装置及部分反应现象如下:
实验装置 |
|
|
|
|
部分实验现象 | a极质量减小、b极质量增加 | 溶液中的SO42-向b极移动 | d极溶解c极有气体产生 | 电子从d极流向a极 |
由此可判断这四种金属的活动性顺序是
A. d>a>b>cB. a>b>c>dC. b>c>d>aD. a>b>d>c
【题目】研究碳、氮及其化合物的转化对于环境的改善有重大意义。
(1)氧化还原法消除NOx的转化如下:NO![]() NO2
NO2![]() N2
N2
已知:NO(g)+O3(g)===NO2(g)+O2(g) ΔH=-200.9 kJ·mol-1
2NO(g)+O2(g)===2NO2(g) ΔH=-116.2 kJ·mol-1
则反应Ⅰ的热化学方程式为___________________________________________________________。
(2)有人设想将CO按下列反应除去:2CO(g)===2C(s)+O2(g) ΔH>0,请你分析该设想能否实现?________(填“能”或“否”),依据是_________________________________________。
(3)一定条件下,CO可与粉末状的氢氧化钠作用生成甲酸钠。已知常温时,甲酸的电离平衡常数Ka=1.70×10-4。
①甲酸钠的水溶液呈碱性,请用离子方程式表示其原因________________________________________。
②向20 mL 0.1 mol·L-1的甲酸钠溶液中滴加10 mL 0.1 mol·L-1的盐酸,混合液呈________(填“酸”或“碱”)性,溶液中离子浓度从大到小的顺序为_________________________________。
(4)活性炭也可用于处理汽车尾气中的NO。在2 L恒容密闭容器中加入0.100 0 mol NO和2.030mol固体活性炭,生成A、B两种气体,在不同温度下测得平衡体系中各物质的物质的量如表所示:
温度 | 固体活性炭/mol | NO/mol | A/mol | B/mol |
200 ℃ | 2.000 | 0.040 0 | 0.030 0 | 0.030 0 |
335 ℃ | 2.005 | 0.050 0 | 0.025 0 | 0.025 0 |
①该反应的正反应为________(填“吸热”或“放热”)反应。
②200 ℃时,平衡后向恒容容器中再充入0.1 mol NO,再次平衡后,NO的百分含量将________(填“增大”“减小”或“不变”)。
③计算反应在335 ℃时的平衡常数为________。





