题目内容
【题目】某校学习小组的同学设计用分子筛催化CH4还原NO2并检验还原产物。回答下列问题:
(1)甲组同学设计用如图所示装置分别制备CH4和NO2。
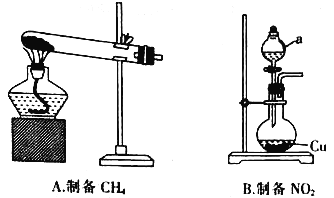
①在加热条件下,无水CH3 COONa与NaOH(CaO为催化剂)生成CH4和Na2CO3的化学方程式为___________。
②仪器a的名称为__________,仪器a中的药品是__________(填名称)。__________(填“能”或“不能”)用铁代替圆底烧瓶中的铜。
(2)乙组同学利用甲组制得的干燥气体并利用下列装置用CH4还原NO2
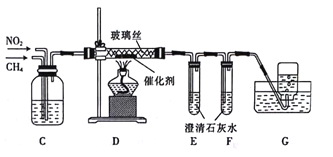
①C装置的作用是______________(列举2点)。
②D装置反应管中盛放玻璃丝的目的是___________;CH4与NO2生成N2和CO2的化学方程式为_____________。
③E装置中澄清石灰水未变浑浊,F装置中澄清石灰水变浑浊,其原因可能是__________。
【答案】CH3COONa+NaOH![]() CH4↑+Na2CO3 分液漏斗 浓硝酸 不能 混合CH4和NO2、调节CH4和NO2的比例(或控制反应的速率) 防止气体将催化剂吹入导管,造成堵塞 CH4+2NO2
CH4↑+Na2CO3 分液漏斗 浓硝酸 不能 混合CH4和NO2、调节CH4和NO2的比例(或控制反应的速率) 防止气体将催化剂吹入导管,造成堵塞 CH4+2NO2![]() N2+CO2+2H2O E中二氧化碳过量,反应生成了碳酸氢钙
N2+CO2+2H2O E中二氧化碳过量,反应生成了碳酸氢钙
【解析】
(1)①根据在加热条件下,无水CH3 COONa与NaOH(CaO为催化剂)生成CH4和Na2CO3书写反应的化学方程式;②根据装置图结合常见仪器的结构解答;实验室可以使用浓硝酸与铜反应制备二氧化氮,铁在常温下遇到浓硝酸发生钝化,据此分析解答;
(2)①在C装置中将CH4和NO2混合均匀,并可以通过气泡的速度调节CH4和NO2的比例和反应速率;②D装置中气体可能将催化剂吹入导管,造成堵塞;CH4与NO2生成N2和CO2,结合质量守恒判断其余生成物,再书写反应的化学方程式;③二氧化碳与澄清石灰水反应生成碳酸钙,若二氧化碳过量,生成的碳酸钙被转化为碳酸氢钙而溶解,据此分析解答。
(1)①在加热条件下,无水CH3 COONa与NaOH(CaO为催化剂)生成CH4和Na2CO3的化学方程式为CH3COONa+NaOH![]() CH4↑+Na2CO3,故答案为:CH3COONa+NaOH
CH4↑+Na2CO3,故答案为:CH3COONa+NaOH![]() CH4↑+Na2CO3;
CH4↑+Na2CO3;
②根据装置图,仪器a为分液漏斗,实验室可以使用浓硝酸与铜反应制备二氧化氮,因此仪器a中的药品为浓硝酸,铁在常温下遇到浓硝酸发生钝化,不能用铁代替圆底烧瓶中的铜,故答案为:分液漏斗;浓硝酸;不能;
(2)①在C装置中将CH4和NO2混合均匀,并可以通过气泡的速率调节CH4和NO2的比例,也可以控制反应的速率,故答案为:混合CH4和NO2;调节CH4和NO2的比例(或控制反应的速率);
②D装置反应管中盛放玻璃丝可以防止气体将催化剂吹入导管,造成堵塞;CH4与NO2生成N2和CO2,反应的化学方程式为CH4+2NO2![]() N2+CO2+2H2O,故答案为:防止气体将催化剂吹入导管,造成堵塞;CH4+2NO2
N2+CO2+2H2O,故答案为:防止气体将催化剂吹入导管,造成堵塞;CH4+2NO2![]() N2+CO2+2H2O;
N2+CO2+2H2O;
③二氧化碳与澄清石灰水反应生成碳酸钙,若二氧化碳过量,生成的碳酸钙被转化为碳酸氢钙而溶解,因此可能造成E装置中澄清石灰水未变浑浊,故答案为:E中二氧化碳过量,生成了碳酸氢钙。

 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案【题目】(1)已知CH3OH(l)的燃烧热ΔH=-238.6 kJ/mol,CH3OH(l)+3/2O2(g)===CO2(g)+2H2O(g)ΔH=-a kJ/mol,则 a___238.6(填“>”、“<”或“=”)。
(2)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1 mol Cl2参与反应时释放出145 kJ热量,写出该反应的热化学方程式:_________________________________。
(3)反应mA(g)+nB(g)![]() pC(g) +qD(g)过程中的能量变化如图所示,回答下列问题。
pC(g) +qD(g)过程中的能量变化如图所示,回答下列问题。
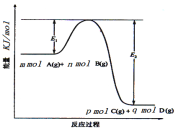
该反应△H =____(用含E1、E2式子表示);在反应体系中加入催化剂,E1___,E2___,(填增大、减小、不变)。
(4)已知:CO (g) +H2O (g)![]() H2 (g) +CO2 (g)平衡常数K随温度的变化如下表:
H2 (g) +CO2 (g)平衡常数K随温度的变化如下表:
温度/℃ | 400 | 500 | 800 |
平衡常数K | 9.94 | 9 | 1 |
回答下列问题:
①该反应的ΔH=__________填“>”、“=”或“<”)。
②已知在一定温度下,C(s) +CO2 (g)![]() 2CO(g)平衡常数K1;C (s) +H2O (g)
2CO(g)平衡常数K1;C (s) +H2O (g)![]() CO(g) +H2 (g)平衡常数K2。则K、K1 、K2之间的关系是__________________________。
CO(g) +H2 (g)平衡常数K2。则K、K1 、K2之间的关系是__________________________。
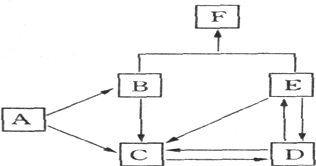
【题目】下面是元素周期表的一部分,请按要求填空:
A | B | C | |||||||||||||||
D | E | F | G | ||||||||||||||
H | I | ||||||||||||||||
(1)A元素的最高价氧化物的电子式______。
(2)元素G在周期表中的位置是_______。
(3)C与D简单离子中半径较大的是________(用离子符号表示)。
(4)C与F的气态氢化物中较稳定是________(用化学式表示)。
(5)写出G单质与I的最高价氧化物对应水化物的溶液反应的化学方程式______。
(6)下列说法或实验不能证明H和I两种元素的金属性强弱的是_____。
a 比较两种元素的单质的熔点、沸点高低
b 将两种元素的单质分别与冷水反应,观察反应的剧烈程度
c 比较两种元素的最高价氧化物对应的水化物的碱性强弱