题目内容
【题目】NA表示阿伏加德罗常数的值。下列说法正确的是
A.39g苯蒸气含碳碳双键的数目为1.5NA
B.将1molNH4NO3溶于适量稀氨水中,所得溶液呈中性,则溶液中NH4+的数目为NA
C.高温下,16.8gFe与足量水蒸气完全反应,转移的电子数为0.45NA
D.电解饱和食盐水消耗2molNaCl,加入含2mol HCl的盐酸可恢复到电解前的状态
【答案】B
【解析】
A. 苯环中不含碳碳双键,故A错误;
B. 根据电荷守恒可知:n(NH4+)+ n(H+)= n(OH-)+ n(NO3-),由于溶液显中性, n(H+)= n(OH-),则n(NH4+)= n(NO3-)=1mol,故溶液中NH4+的数目为NA,故B正确;
C. 铁与水蒸气反应:3Fe+4H2O![]() Fe3O4+3H2,3molFe参与反应,转移了8mol电子,16.8gFe的物质的量为0.3mol,即转移0.8mol电子,故C错误;
Fe3O4+3H2,3molFe参与反应,转移了8mol电子,16.8gFe的物质的量为0.3mol,即转移0.8mol电子,故C错误;
D. 电解饱和食盐水消耗2molNaCl,从阳极析出的是1mol氯气,阴极析出的是1mol氢气,故若使溶液复原,应加入2molHCl气体,不能加入盐酸,故D错误;
故选:B。

 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
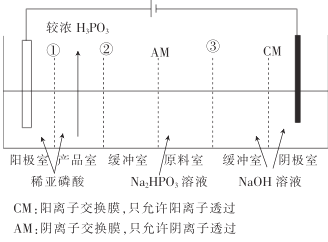
海淀课时新作业金榜卷系列答案【题目】磷是重要的元素,能形成多种含氧酸。回答下列问题:
(1)次磷酸(H3PO2)是一元酸,其电离常数的值K=9×103。向10mL0.1 molL-1H3PO2溶液中加入30mL等物质的量浓度的NaOH溶液,写出反应的离子方程式_________,c(Na+)+(H2PO2-)+c(H3PO2)=______(忽略混合后溶波体积的变化)。
(2)亚磷酸(H3PO3)是二元弱酸, 25℃时亚磷酸的电离常数的值为K1=1×10-2、k2=2.6×10-7,则NaH2PO3溶液显性_____(填“酸”“碱”或“中”),原因是____(结合化学用语及数据计算进行解释)
(3)已知HF的电离常数的值为K=3.6×10-4,将足量HF溶液和Na2HPO3溶液反应,其离子方程式为______。
(4)亚磷酸具有强还原性。化学实验小组利用滴定法测定某亚磷酸溶液的浓度,取25.00mL的亚磷酸溶液放入锥形瓶中,用0.10 molL-1的高锰酸钾溶液进行滴定,反应的离子方程式是5H3PO3+ 2MnO4-+6H+ = 5H3PO4+ 2Mn2+ +3H2O。
三次滴定实验的数据分别如下:
实验编号 | 滴定前读数 | 滴定后读数 |
1 | 0.50 | 22.50 |
2 | 1.50 | 24.50 |
3 | 1.00 | 22.00 |
①亚磷酸溶液的物质的量浓度为______。
②关于该实验下列说法正确的是______(填写序号)。
a 取亚磷酸溶液的滴定管,洗涤后未润洗,导致结果偏低
b 盛高锰酸钾溶液的滴定管滴定前有气泡,滴定后无气泡,导致结果偏高
c 滴定过程中眼睛只注视滴定管中液面变化,并做好记录
d 锥形瓶未干燥底部有水,会导致结果偏低