题目内容
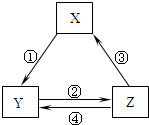 下表各组物质之间通过一步反应不可以实现如图所示转化关系的是( )
下表各组物质之间通过一步反应不可以实现如图所示转化关系的是( )| 选项 | X | Y | Z | 箭头上所标 数字的反应条件 |
| A | SiO2 | Na2SiO3 | H2SiO3 | ①与Na2CO3熔融 |
| B | NaCl | NaHCO3 | Na2CO3 | ②加热 |
| C | N2 | NO2 | HNO3 | ③加热 |
| D | C | CO | CO2 | ④灼热炭粉 |
| A、A | B、B | C、C | D、D |
考点:硅和二氧化硅,含氮物质的综合应用,金属的通性
专题:氮族元素,碳族元素,几种重要的金属及其化合物
分析:A.二氧化硅和碳酸钠熔融生成硅酸钠,硅酸钠和稀盐酸反应生成硅酸,硅酸分解生成二氧化硅;
B.氯化钠和氨气、二氧化碳反应生成碳酸氢钠,碳酸氢钠加热分解生成碳酸钠,碳酸钠和二氧化碳、水反应生成碳酸氢钠,碳酸钠和氯化钙反应生成氯化钠;
C.氮气和氧气反应生成NO而不能生成二氧化氮;硝酸分解生成二氧化氮、氧气和水;
C.碳不完全燃烧生成CO,CO燃烧生成二氧化碳,二氧化碳和C反应生成CO,二氧化碳和镁反应生成C.
B.氯化钠和氨气、二氧化碳反应生成碳酸氢钠,碳酸氢钠加热分解生成碳酸钠,碳酸钠和二氧化碳、水反应生成碳酸氢钠,碳酸钠和氯化钙反应生成氯化钠;
C.氮气和氧气反应生成NO而不能生成二氧化氮;硝酸分解生成二氧化氮、氧气和水;
C.碳不完全燃烧生成CO,CO燃烧生成二氧化碳,二氧化碳和C反应生成CO,二氧化碳和镁反应生成C.
解答:
解:A.二氧化硅和碳酸钠熔融生成硅酸钠,硅酸钠和稀盐酸反应生成硅酸,硅酸分解生成二氧化硅,涉及的反应为 SiO2+Na2CO3
Na2SiO3+CO2↑、Na2SiO3+2HCl=2NaCl+H2SiO3↓、H2SiO3
H2O+SiO2,故A正确;
B.氯化钠和氨气、二氧化碳反应生成碳酸氢钠,碳酸氢钠加热分解生成碳酸钠,碳酸钠和二氧化碳、水反应生成碳酸氢钠,碳酸钠和氯化钙反应生成氯化钠,发生的反应为NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl、2NaHCO3
Na2CO3+H2O+CO2↑、Na2CO3+H2O+CO2=2NaHCO3、Na2CO3+CaCl2=CaCO3↓+2NaCl,故B正确;
C.氮气和氧气反应生成NO而不能生成二氧化氮;硝酸分解生成二氧化氮、氧气和水,发生的反应为N2+O2
2NO、3NO2+H2O=2HNO3+NO、4HNO3
4NO2↑+O2↑+2H2O,故C错误;
C.碳不完全燃烧生成CO,CO燃烧生成二氧化碳,二氧化碳和C反应生成CO,二氧化碳和镁反应生成C,发生的反应为2C+O2
2CO、2CO+O2
2CO2、C+CO2
2CO、CO2+2Mg
2MgO+C,故D正确;
故选C.
| ||
| ||
B.氯化钠和氨气、二氧化碳反应生成碳酸氢钠,碳酸氢钠加热分解生成碳酸钠,碳酸钠和二氧化碳、水反应生成碳酸氢钠,碳酸钠和氯化钙反应生成氯化钠,发生的反应为NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl、2NaHCO3
| ||
C.氮气和氧气反应生成NO而不能生成二氧化氮;硝酸分解生成二氧化氮、氧气和水,发生的反应为N2+O2
| ||
| ||
C.碳不完全燃烧生成CO,CO燃烧生成二氧化碳,二氧化碳和C反应生成CO,二氧化碳和镁反应生成C,发生的反应为2C+O2
| ||
| ||
| ||
| ||
故选C.
点评:本题考查了元素化合物中物质之间的转化,明确物质的性质是解本题关键,知道哪些物质之间能直接发生反应,注意反应条件,知道镁能在二氧化碳中燃烧,为易错点.

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目
下列关于同系物的说法中,错误的是( )
| A、同系物具有相同的分子式 |
| B、同系物符合同一通式 |
| C、相邻的同系物彼此在组成上相差一个CH2原子团 |
| D、同系物的化学性质基本相似 |
0.02mol氯化铬(CrCl3?6H2O)在水溶液中用过量的AgNO3处理,产生0.04mol AgCl沉淀,此氯化铬最可能形成的是( )
| A、[Cr(H2O)6]Cl3 |
| B、[Cr(H2O)3Cl3]?3H2O |
| C、[Cr(H2O)4Cl2]Cl?2H2O |
| D、[Cr(H2O)5Cl]Cl2?H2O |
要得到较大颗粒的明矾晶体,在结晶时可如下操作( )
| A、配制比室温高10~20℃明矾饱和溶液然后浸入悬挂的明矾小晶核,静置过夜 |
| B、在沸水中配制明矾饱和溶液,然后急速冷却结晶 |
| C、室温下,在明矾饱和溶液中投入明矾小晶核,静置过夜 |
| D、进行快速蒸发明矾饱和溶液至大量晶体析出 |
既有氧化性、又有还原性的物质是( )
| A、SO2 |
| B、SO3 |
| C、Na |
| D、Fe3+ |
下列说法正确的是( )
| A、凡是中心原子采取sp3杂化的分子,其立体构形都是正四面体 |
| B、CH4分子中的sp3杂化轨道是由4个H原子的1s轨道和C原子的2p轨道混合起来而形成的 |
| C、杂化轨道只用于形成σ键或用于容纳未参与成键的孤电子对 |
| D、凡AB3型的共价化合物,其中心原子A均采用sp3杂化轨道成键 |
生物体中细胞膜内的葡萄糖,细胞膜外的富氧液体及细胞膜构成微型的生物原电池,下列有关判断正确的是( )
| A、负极发生的电极反应可能是:O2-4e-+2H2O═4OH- |
| B、正极发生的电极反应可能是:O2-4e-═2O2- |
| C、负极反应主要是C6H12O6生成CO2或HCO3- |
| D、正极反应主要是C6H12O6生成CO2或CO32- |
近年来,加“碘”食盐较多使用碘酸钾,KIO3在工业上可用电解法制取,以石墨和铁为电极,以KI溶液为电解液在一定条件下电解,反应式为KI+H2O→KIO3+H2↑(未配平).下列有关说法中,正确的是( )
| A、电解时,石墨做阴极,铁作阳极 |
| B、电解时,在阳极上产生氢气 |
| C、电解后得到KIO3产品的步骤有:过滤→浓缩→结晶→灼烧 |
| D、电解中,每转移0.6mol电子,理论上可得到0.1mol无水KIO3晶体 |