题目内容
下列各溶液中,叙述正确的是
| A.0.1mol/L的(NH4)2SO4溶液中:c(SO42-)>c(NH4+)>c(H+)>c(OH-) |
| B.25℃时,将pH=3的盐酸溶液和pH=11的氨水等体积混合后,溶液中离子浓度的大小关系:c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
| C.将0.1mol/L醋酸溶液加大量水稀释后,溶液的pH增大 |
| D.Na2CO3溶液中:c(Na+ )="2c" (CO32- ) + c (HCO3- ) + c (H2CO3 ) |
C
解析试题分析:A、硫酸铵是强酸弱碱盐,NH4+水解溶液显酸性,但水解程度很小,NH4+浓度大于SO42-浓度,即c(NH4+)>c(SO42-)>c(H+)>c(OH-),A不正确;B、盐酸是强酸,氨水是弱碱,因此25℃时,将pH=3的盐酸溶液和pH=11的氨水等体积混合后氨水过量,溶液显碱性,溶液中离子浓度的大小关系:c(NH4+)>c(Cl-)>c(OH-)>c(H+),B不正确;C、醋酸是弱酸存在电离平衡,稀释促进电离,但溶液的酸性仍然是减小的,所以将0.1mol/L醋酸溶液加大量水稀释后,溶液的pH增大,C正确;D、根据物料守恒可知Na2CO3溶液中:c(Na+ )="2c" (CO32- ) + 2c (HCO3- ) + 2c (H2CO3 ),D不正确,答案选C。
考点:考查溶液中离子浓度大小比较

练习册系列答案
相关题目
室温下,将0.100 0 mol·L-1盐酸滴入20.00 ml 未知浓度的某一元碱MOH溶液中,溶液pH随加入盐酸体积变化曲线如图。下列有关说法不正确的是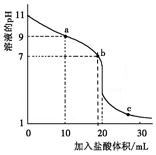
| A.该一元碱溶液浓度为0.100 0 mol·L-1 |
| B.a、b、c点的水溶液导电性依次增强 |
| C.室温下,MOH的电离常数Kb=1×10-5 |
| D.b点:c(M+)+c(MOH)=c(Clˉ) |
室温下,对于0.10 mol·L-1的氨水,下列判断正确的是( )
| A.与AlCl3溶液发生反应的离子方程式为Al3++3OH-=Al(OH)3↓ |
| B.加水稀释后,溶液中c(NH4+)·c(OH-)变大 |
| C.用HNO3溶液完全中和后,溶液不显中性 |
| D.其溶液的pH=13 |
在蒸发皿中用酒精灯加热蒸干下列物质的溶液然后灼烧,可以得到该物质固体的是( )
| A.AlCl3 | B.Na2SO3 | C.KMnO4 | D.MgSO4 |
下列关于电解质溶液的叙述正确的是( )
A.常温下,由0.1 mol·L-1一元碱BOH溶液的pH=10,可推知BOH溶液存在:BOH B++OH- B++OH- |
| B.常温下,pH=7的NH4Cl与氨水的混合溶液中:c(Cl-)>c(NH4+)>c(H+)=c(OH-) |
| C.中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同 |
| D.将pH=4的盐酸稀释后,溶液中所有离子的浓度均降低 |
在Na2CO3溶液中,下列离子浓度的关系正确的是 ( )。
| A.c(Na+)=2c(CO32-) | B.c(H+)>c(OH-) |
| C.c(CO32-)<c(HCO3-) | D.c(OH-)>c(H+) |
下列事实不能说明醋酸是弱电解质的是( )
| A.0.1 mol·L-1醋酸的pH比0.1 mol·L-1盐酸的pH大 |
| B.醋酸能和碳酸钙反应放出CO2 |
| C.0.1 mol·L-1醋酸钠溶液的pH=8.9 |
| D.大小相同的锌粒分别与相同物质的量浓度的盐酸和醋酸反应,醋酸产生H2速率慢 |
下列说法正确的是( )
| A.pH=4的溶液中水电离出的H+一定是1×10-4mol/L |
| B.25 ℃时,用醋酸溶液滴定等浓度NaOH溶液至pH=7,V醋酸<VNaOH |
| C.向NaAlO2溶液中滴加NaHCO3溶液,有沉淀和气体生成 |
| D.AgCl沉淀易转化为AgI沉淀且K(AgX)=c(Ag+)·c(X-),故K(AgI)<K(AgCl) |