题目内容
在Na2CO3溶液中,下列离子浓度的关系正确的是 ( )。
| A.c(Na+)=2c(CO32-) | B.c(H+)>c(OH-) |
| C.c(CO32-)<c(HCO3-) | D.c(OH-)>c(H+) |
D
解析

练习册系列答案
相关题目
下列各溶液中,叙述正确的是
| A.0.1mol/L的(NH4)2SO4溶液中:c(SO42-)>c(NH4+)>c(H+)>c(OH-) |
| B.25℃时,将pH=3的盐酸溶液和pH=11的氨水等体积混合后,溶液中离子浓度的大小关系:c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
| C.将0.1mol/L醋酸溶液加大量水稀释后,溶液的pH增大 |
| D.Na2CO3溶液中:c(Na+ )="2c" (CO32- ) + c (HCO3- ) + c (H2CO3 ) |
一定温度下,卤化银AgX(X:Cl—、Br—、I—)及Ag2CrO4的沉淀溶解平衡曲线如图所示。横坐标p(Ag+)表示“-lgc(Ag+)”,纵坐标Y表示“ -lgc(X-)”或“-lgc(CrO42—)”。下列说法正确的是
| A.a点表示c(Ag+)=c(CrO42—) |
| B.b点可表示AgI的饱和溶液 |
| C.该温度下AgI的Ksp约为1×10—16 |
| D.该温度下AgCl、AgBr饱和溶液中:c(Cl—)<c(Br—) |
常温下,Ksp(CaSO4)=9´10-6,常温下CaSO4在水中的沉淀溶解平衡曲线见图。下列说法正确的是( )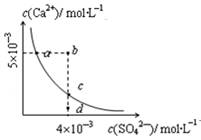
| A.在任何溶液中,c(Ca2+)、c(SO42-)均相等 |
| B.d点溶液通过蒸发可以变到c点 |
| C.a点对应的Ksp等于c点对应的Ksp |
| D.b点将有沉淀生成,平衡后溶液中c(SO42-)一定等于4´10-3 mol·L-1 |
下列实验现象、解释与结论均正确的是
| 编号 | 实验操作 | 实验现象 | 解释与结论 |
| A | 铜与浓硝酸反应,生成气体用湿润KI-淀粉试纸检验 | 试纸变蓝 | NO2为酸性气体 |
| B | 向某溶液中加入稀盐酸酸化的BaCl2溶液 | 有白色沉淀产生 | 该沉淀可能是BaSO4,该溶液中可能含有SO42- |
| C | 向甲苯中滴入少量浓溴水,振荡,静置 | 溶液分层,上层呈橙红色,下层几乎无色 | 甲苯和溴水发生取代反应,使溴水褪色 |
| D | 在稀AgNO3溶液中先加入过量0.1mol/L NaCl溶液,再加入少量0.1mol/L NaI溶液 | 先产生白色沉淀,后出现黄色沉淀 | 说明Ksp(AgCl)>Ksp(AgI) |
室温下,用0.100 mol/L NaOH 溶液分别滴定20.00 mL 0.100 mol/L的盐酸和醋酸,滴定曲线如下图所示。下列说法正确的是( )
| A.Ⅰ、Ⅱ分别表示盐酸和醋酸的滴定曲线 |
B.V(NaOH)=10.00 mL 时, >1 >1 |
| C.pH=7时,两种酸所用NaOH溶液的体积相等 |
| D.V(NaOH)=20 .00 mL 时,c(Cl-)<c(CH3COO-) |
现有pH=5的CH3COOH溶液10 mL,要使其pH增大3,可采取的方法有( )
| A.向溶液中加水稀释至10 L |
| B.加入一定量的NaOH固体 |
| C.加入一定量pH=8的NaOH溶液 |
| D.加入一定浓度的盐酸 |
常温下,0.1 mol·L-1 HX溶液的pH=1,0.1 mol·L-1 CH3COOH溶液的pH=2.9。下列说法不正确的是 ( )。
| A.HX和CH3COOH均可抑制水的电离 |
| B.取HCl与HX各0.1 mol溶于水配制成1 L混合溶液,则溶液的c(H+)=0.2 mol·L-1 |
| C.等物质的量浓度、等体积的HX溶液与CH3COONa溶液混合后所得的溶液中:c(Na+)>c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-) |
| D.向等物质的量浓度、等体积的HX溶液和CH3COOH溶液中,分别加入一定物质的量浓度的NaOH溶液,欲使两者的pH均等于7,则消耗氢氧化钠溶液的体积:前者大于后者 |
向0.1 mol/L的CH3COOH溶液中加水或加入少量CH3COONa晶体时,下列有关叙述不正确的是( )
| A.都能使溶液的pH增加 |
| B.都能使溶液中c(H+)·c(CH3COO-)增大 |
C.都能使溶液中 比值增大 比值增大 |
| D.溶液中c(H+)·c(OH-)不变 |