题目内容
【题目】糖类、油脂、蛋白质是人体重要的能源物质,请根据它们的性质回答以下问题:
(1)油脂在酸性和碱性条件下水解的共同产物是________________(写名称)。
(2)蛋白质的水解产物具有的官能团是____________________(写结构简式)。
已知A是人体能消化的一种天然高分子化合物,B和C分别是A在不同条件下的水解产物,它们有如下转化关系,请根据该信息完成(3)~(5)小题。
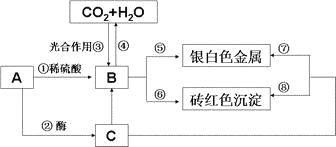
(3)下列说法不正确的是______________________
A.1molC完全水解可生成2molB
B.工业上常利用反应⑦给热水瓶胆镀银
C.用A进行酿酒的过程就是A的水解反应过程
D.A的水溶液可以发生丁达尔效应
E. 反应③属于吸热反应
(4)1molB完全氧化时可以放出2804kJ的热量,请写出其氧化的热化学方程式___________________。
(5)请设计实验证明A通过反应①已经全部水解,写出操作方法、现象和结论:____________________________________________________________________。
【答案】甘油(或丙三醇) -NH2、-COOH BC C6H12O6(s) +6O2(g) =6CO2(g)+6H2O(l) △H=-2804kJ/mol 取少量淀粉水解后的溶液,向其中加入碘水,若溶液不变蓝证明淀粉已经全部水解
【解析】
(1)油脂在酸性条件下水解成高级脂肪酸和甘油,在碱性条件下水解成高级脂肪酸盐和甘油,油脂在酸性和碱性条件下水解的共同产物是甘油(或丙三醇);
(2)蛋白质水解的产物是氨基酸,氨基酸中的官能团为—NH2和—COOH,蛋白质的水解产物具有的官能团是—NH2和—COOH;
(3)根据图,B是光合作用的产物,A是人体能消化的一种天然高分子化合物,B和C分别是A在不同条件下的水解产物,可以推断出A为淀粉,B为葡萄糖,C为麦芽糖;
A项,1mol麦芽糖完全水解可生成2mol葡萄糖,故A正确;
B项,工业上常利用葡萄糖的银镜反应给热水瓶镀银,即利用反应⑤的原理给热水瓶胆镀银,故B错误;
C项,A的水解反应过程生成了葡萄糖,葡萄糖在酒化酶的作用下反应生成乙醇和CO2,不是淀粉水解成乙醇,故C错误;
D项,A为淀粉,淀粉溶液属于胶体,所以可以发生丁达尔效应,故D正确;
E项,反应③将光能转化为化学能,属于吸热反应,故E正确;
答案选BC;
(4)葡萄糖燃烧后生成了水和二氧化碳,其反应的热化学方程式为:C6H12O6(s) +6O2(g) =6CO2(g)+6H2O(l) △H=-2804kJ/mol;
(5)要证明淀粉已经全部水解,即证明水解液中不含淀粉,故检验的方法为:取少量淀粉水解后的溶液,向其中加入碘水,若溶液不变蓝证明淀粉已经全部水解。

【题目】用零价铁(Fe)去除水体中的硝酸盐(NO3-)已成为环境修复研究的热点之一。
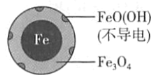
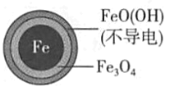
(1)Fe还原水体中NO3-的反应原理如图所示。
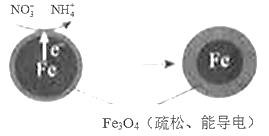
①作负极的物质是____。
②正极的电极反应式是____。
(2)将足量铁粉投入水体中,经24小时测定NO3-的去除率和pH,结果如下:
初始pH | pH=2.5 | pH=4.5 |
NO3-的去除率 | 接近100% | <50% |
24小时pH | 接近中性 | 接近中性 |
铁的最终物质形态 |
|
|
pH=4.5时,NO3-的去除率低。其原因是____。
(4)其他条件与(2)相同,经1小时测定NO3-的去除率和pH,结果如下:
初始pH | pH=2.5 | pH=4.5 |
NO3-的去除率 | 约10% | 约3% |
1小时pH | 接近中性 | 接近中性 |
与(2)中数据对比,解释(2)中初始pH不同时,NO3-去除率和铁的最终物质形态不同的原因:____。
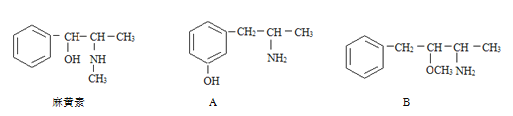
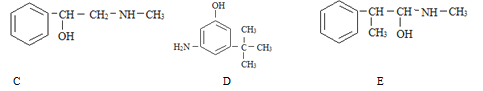
【题目】(1)麻黄素又称黄碱,是我国特定的中药材麻黄中所含有的一种生物碱。经我国科学家研究发现其结构如下图,下列各物质与麻黄素互为同分异构体的是_____(填字母,下同),互为同系物的是_____。
(2)烷基取代苯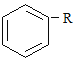 可以被KMnO4的酸性溶液氧化生成
可以被KMnO4的酸性溶液氧化生成 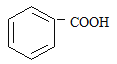 ,但若烷基R中直
,但若烷基R中直
接与苯环连接的碳原子上没有C一H键,则不容易被氧化得到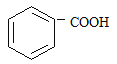 。 现有分子式是C11H16的一烷基取代苯,已知它可以被氧化成为的异构体共有7种,其中的3种是
。 现有分子式是C11H16的一烷基取代苯,已知它可以被氧化成为的异构体共有7种,其中的3种是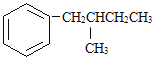
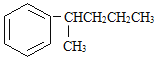
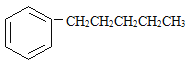
写出另4种的结构简式:
1________ | 2________ |
3________ | 4________ |
【题目】一定温度时,向2.0 L恒容密闭容器中充入2 mol SO2和1 mol O2,发生反应:2SO2(g)+O2(g)![]() 2SO3(g)。经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
2SO3(g)。经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
t / s | 0 | 2 | 4 | 6 | 8 |
n(SO3) / mol | 0 | 0.8 | 1.4 | 1.8 | 1.8 |
下列说法正确的是( )
A. 反应在前2 s 的平均速率v(O2) = 0.4 mol·L-1·s-1
B. 保持其他条件不变,体积压缩到1.0 L,平衡常数将增大
C. 相同温度下,起始时向容器中充入4 mol SO3,达到平衡时,SO3的转化率小于10%
D. 保持温度不变,向该容器中再充入2 mol SO2、1 mol O2,反应达到新平衡时n(SO3)/n(O2)减小