题目内容
11.化学与材料、生活和环境密切相关.下列有关说法中错误的是( )| A. | 利用CO2合成聚碳酸酯类可降解塑料,实现“碳”的循环利用 | |
| B. | 日常生活中人们大量使用铝制品,是因为常温下铝不能与氧气反应 | |
| C. | 煤炭经气化、液化和干馏等过程,可获得清洁能源和重要的化工原料 | |
| D. | 神舟10号飞船所用太阳能电池板可将光能转换为电能,所用转换材料是单晶硅 |
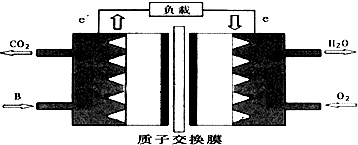
分析 A.利用CO2合成聚碳酸酯类可降解塑料,实现“碳”的循环利用应用,减少二氧化碳的排放;
B.铝性质活泼,常温下,铝极易和氧气反应生成氧化铝;
C.煤炭经气化、液化和干馏可获得清洁能源和重要的化工原料;
D.太阳能电池的材料是硅单质;
解答 解:A.利用CO2合成聚碳酸酯类可降解塑料,实现“碳”的循环利用应用,减少二氧化碳的排放,符合节能减排的原则,故A正确;
B.Al属于亲氧元素,常温下,铝极易和氧气反应生成氧化铝从而阻止铝进一步被氧化,故B错误;
C.煤的气化是煤在氧气不足的条件下进行部分氧化形成H2、CO等气体的过程;煤的液化是将煤与H2在催化剂作用下转化为液体燃料或者利用煤产生的H2和CO通过化学合成产生液体燃料或者其他液体化工产品的过程;煤的干馏是指隔绝空气加强热,使煤分解的过程,可以得到很多重要的化工原料,故C正确;
D.太阳能电池板的材料是硅单质,故D正确;
故选:B.
点评 本题考查了物质的用途、物质的性质及煤的加工,明确物质的性质是解本题关键,注意对基础知识的理解掌握.

练习册系列答案
相关题目
1.将0.2moL/L的CH3COONa溶液与0.1mol/L的硝酸溶液等体积混合后,溶液中下列粒子的物质的量浓度的关系正确的是( )
| A. | c(CH3COO-)+c(NO3-)+c(OH-)=c(H+)+c(Na+) | |
| B. | c(CH3COO-)=c(Na+)=c(NO3-)>c(CH3COOH)>c(H+)>c(Na+) | |
| C. | c(CH3COO-)>c(NO3-)>c(CH3COOH)=c(Na+)>c(H+)>c(OH-) | |
| D. | c(Na+)>c(NO3-)>c(CH3COO-)>c(CH3COOH)>c(H+)>c(OH-) |
19.用NA表示阿伏加德罗常数的值,下列叙述正确的是(Cu-64 O-16)( )
| A. | 1molNa2O2晶体中阴离子的个数为2NA | |
| B. | 标准状况下,2.24L苯所含的分子总数为0.1NA | |
| C. | 32gO2和32g O3的所含的氧原子数都是为2NA | |
| D. | 6.4g铜与过量的浓硝酸完全反应转移的电子数是0.1NA |
6.有五种短周期主族元素X、Y、Z、W、Q,其中Q的单质是密度最小的气体,X原子的最外层电子数是内层电子数的2倍,Y和W同主族且原子序数之比为2:1,Z是短周期中原子半径最大的元素.下列叙述错误的是( )
| A. | XQ2W分子在常温下呈气态,分子中的四个原子在同一平面内 | |
| B. | Z和W形成的两种离子化合物中阴、阳离子个数比均为2:1 | |
| C. | X、W两元素分别和Q元素化合,可形成电子数相同的两种化合物 | |
| D. | 相应的离子半径大小关系为:Y>W>Z |
3.25℃时,下列各组离子在指定溶液中能大量共存的是( )
| A. | pH=1的溶液中:Na+、NH4+、SO42-、ClO- | |
| B. | KW/c(H+)=0.1 mol•L-1的溶液中:Na+、K+、MnO4-、HCO3- | |
| C. | 0.1 mol•L-1的Na2SO3溶液中:K+、H+、SO42-、NO3- | |
| D. | 澄清透明的溶液中:Fe3+、Na+、Cl-、SO42- |
 ,
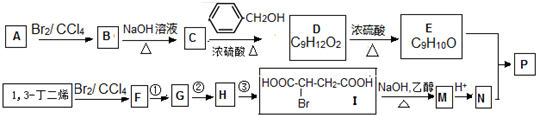
,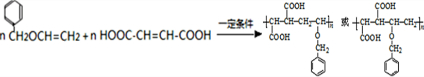 高聚物P的亲水性比由E形成的聚合物强(填“强、弱”).
高聚物P的亲水性比由E形成的聚合物强(填“强、弱”).
 用化学用语回答下面的问题
用化学用语回答下面的问题