题目内容
16.共聚法可改进有机高分子化合物的性质,高分子聚合物P的合成路线如下: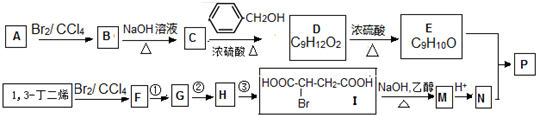
(1)B的名称为1,2-二溴乙烷,E中所含官能团的名称为醚键、碳碳双键
(2)I由F经①~③合成,F可以使溴水褪色.
a.①的化学方程式是
 ,
,b.②的反应试剂是HBr
c.③的反应类型是氧化反应
(3)下列说法正确的是ac
a.C可与水任意比例混合
b.A与1,3-丁二烯互为同系物
c.由I生成M时,1mol最多消耗3molNaOH
d.N不存在顺反异构体
(4)写出E与N按照物质的量之比为1:1发生共聚生成P的化学反应方程式:
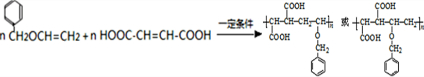 高聚物P的亲水性比由E形成的聚合物强(填“强、弱”).
高聚物P的亲水性比由E形成的聚合物强(填“强、弱”).(5)D的同系物K比D分子少一个碳原子,K 有多种同分异构体,符合下列条件的K的同分异构体有9种,写出其中核磁共振氢谱为1:2:2:2:3的一种同分异构体的结构简式

a.苯环上有两种等效氢
b.能与氢氧化钠溶液反应
c.一定条件下1mol该有机物与足量金属钠充分反应,生成1molH2.
分析 A和溴发生加成反应生成B,B和氢氧化钠的水溶液发生取代反应生成C,C和苯甲醇反应生成D,A、B和C中碳原子个数相同,根据D的分子式知,A中含有两个碳原子,则A是CH2=CH2,B是BrCH2CH2Br,C是HOCH2CH2OH,D的结构简式为: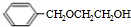 ,对比D、E分子式可知,D发生消去反应生成E,则E的结构简式为:
,对比D、E分子式可知,D发生消去反应生成E,则E的结构简式为: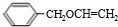 .根据I的结构简式知,1,3-丁二烯和溴发生1,4-加成生成F为BrCH2CH=CHCH2Br,F在氢氧化钠的水溶液、加热条件下发生取代反应生成G为:HOCH2CH=CHCH2OH,G和HBr发生加成反应生成H为HOCH2CH2CHBrCH2OH,H被酸性高锰酸钾氧化生成I,I和氢氧化钠的醇溶液发生消去反应生成M为:NaOOCCH=CHCOONa,然后酸化得到N,则N的结构简式为:HOOCCH=CHCOOH,E和N发生加聚反应生成P,则P的结构简式为:
.根据I的结构简式知,1,3-丁二烯和溴发生1,4-加成生成F为BrCH2CH=CHCH2Br,F在氢氧化钠的水溶液、加热条件下发生取代反应生成G为:HOCH2CH=CHCH2OH,G和HBr发生加成反应生成H为HOCH2CH2CHBrCH2OH,H被酸性高锰酸钾氧化生成I,I和氢氧化钠的醇溶液发生消去反应生成M为:NaOOCCH=CHCOONa,然后酸化得到N,则N的结构简式为:HOOCCH=CHCOOH,E和N发生加聚反应生成P,则P的结构简式为: .
.
解答 解:A和溴发生加成反应生成B,B和氢氧化钠的水溶液发生取代反应生成C,C和苯甲醇反应生成D,A、B和C中碳原子个数相同,根据D的分子式知,A中含有两个碳原子,则A是CH2=CH2,B是BrCH2CH2Br,C是HOCH2CH2OH,D的结构简式为: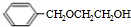 ,对比D、E分子式可知,D发生消去反应生成E,则E的结构简式为:
,对比D、E分子式可知,D发生消去反应生成E,则E的结构简式为: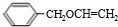 .根据I的结构简式知,1,3-丁二烯和溴发生1,4-加成生成F为BrCH2CH=CHCH2Br,F在氢氧化钠的水溶液、加热条件下发生取代反应生成G为:HOCH2CH=CHCH2OH,G和HBr发生加成反应生成H为HOCH2CH2CHBrCH2OH,H被酸性高锰酸钾氧化生成I,I和氢氧化钠的醇溶液发生消去反应生成M为:NaOOCCH=CHCOONa,然后酸化得到N,则N的结构简式为:HOOCCH=CHCOOH,E和N发生加聚反应生成P,则P的结构简式为:
.根据I的结构简式知,1,3-丁二烯和溴发生1,4-加成生成F为BrCH2CH=CHCH2Br,F在氢氧化钠的水溶液、加热条件下发生取代反应生成G为:HOCH2CH=CHCH2OH,G和HBr发生加成反应生成H为HOCH2CH2CHBrCH2OH,H被酸性高锰酸钾氧化生成I,I和氢氧化钠的醇溶液发生消去反应生成M为:NaOOCCH=CHCOONa,然后酸化得到N,则N的结构简式为:HOOCCH=CHCOOH,E和N发生加聚反应生成P,则P的结构简式为: .
.
(1)B的结构简式为BrCH2CH2Br,其名称是1,2-二溴乙烷,E的结构简式为: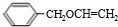 ,其官能团名称为醚键、碳碳双键,
,其官能团名称为醚键、碳碳双键,
故答案为:1,2-二溴乙烷;醚键、碳碳双键;
(2)a.反应①的化学方程式是: ,
,
b.反应②的试剂是HBr;
c.H发生氧化反应生成生成I,
故答案为: ;HBr;氧化反应;
;HBr;氧化反应;
(3)a.C是乙二醇,可与水以任意比例混溶,故正确;
b.A是乙烯,乙烯与1,3-丁二烯结构不同,所以不互为同系物,故错误;
c.I生成M时,1mol I最多消耗3mol NaOH,故正确;
d.N的结构简式为:HOOCCH=CHCOOH,N存在顺反异构体,故错误;
故选:ac;
(4)E的结构简式为: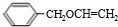 ,N的结构简式为:HOOCCH=CHCOOH,二者以1:1发生加成反应生成P,反应方程式为
,N的结构简式为:HOOCCH=CHCOOH,二者以1:1发生加成反应生成P,反应方程式为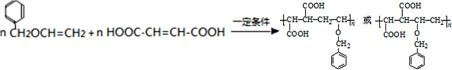 ,
,
P的结构简式为 ,E的结构简式为
,E的结构简式为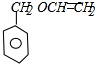 ,P中含有亲水基,E不含亲水基,所以高聚物P的亲水性比由E形成的聚合物强,
,P中含有亲水基,E不含亲水基,所以高聚物P的亲水性比由E形成的聚合物强,
故答案为: ;强;
;强;
(5)D的结构简式为: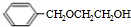 ,D的同系物K比D分子少一个碳原子,K有多种同分异构体,同分异构体符合下列条件:a.苯环上有两种等效氢,说明苯环上有两种类型的H原子;b.能与氢氧化钠溶液反应,说明含有酚羟基;c.一定条件下1mol该有机物与足量金属钠充分反应,生成1mol H2,说明含有两个羟基,
,D的同系物K比D分子少一个碳原子,K有多种同分异构体,同分异构体符合下列条件:a.苯环上有两种等效氢,说明苯环上有两种类型的H原子;b.能与氢氧化钠溶液反应,说明含有酚羟基;c.一定条件下1mol该有机物与足量金属钠充分反应,生成1mol H2,说明含有两个羟基,
如果K的同分异构体中含有1个酚羟基、1个醇羟基时,醇羟基有-CH2CH2OH、-CH(OH)CH3,与酚羟基处于对位,则K有2种同分异构体;
当苯环上有2个酚羟基、1个乙基时,2个酚羟基和乙基位于相邻位置且乙基处于中间,可以是三个取代基处于间位,K有2种同分异构体;
当苯环上有2个酚羟基、2个甲基时,2个酚羟基相邻、2个甲基相邻且4个取代基相邻,或者4个取代基相邻且甲基与酚羟基交叉相邻,或者两个甲基、1个羟基相邻且另外1个羟基处于间位、其对位为甲基,或者两个羟基、1个甲基相邻且另外1个甲基处于间位、其对位为羟基,或者两个甲基处于间位、2个羟基位于甲基的对位,K有5种同分异构体;
所以符合条件的同分异构体有9种;其中核磁共振氢谱为1:2:2:2:3的一种同分异构体的结构简式为 ,
,
故答案为:9; .
.
点评 本题考查了有机物推断充分利用转化关系中物质的结构、反应条件进行推断,需要学生熟练掌握官能团的性质与转化,较好的考查学生分析推理能力,(5)中同分异构体书写为易错点、难点,题目难度中等.

 高效智能课时作业系列答案
高效智能课时作业系列答案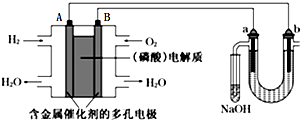
| A. | 电池工作时,B极反应式为O2+2H2O+4e-=4OH- | |
| B. | 电解时,电子流动路径是:A极→外电路→b极→溶液→a极→B极 | |
| C. | NaOH溶液充分吸收后所得溶液可制作漂白水 | |
| D. | 当电池中消耗2.24L(标准状况)H2时,a极周围也会产生2.24L(标准状况)气体 |
| A. | 葡萄糖氯化钠注射液--用于补充热能和体液 | |
| B. | 二氧氯(ClO2)或漂白粉--利用其氧化性对居所和饮用水消毒 | |
| C. | 络合碘--碘化钾的水溶液,可以用于皮肤和粘膜的消毒 | |
| D. | 电池--通常选用干电池,用于小功率电器的供电 |
| A. | 利用CO2合成聚碳酸酯类可降解塑料,实现“碳”的循环利用 | |
| B. | 日常生活中人们大量使用铝制品,是因为常温下铝不能与氧气反应 | |
| C. | 煤炭经气化、液化和干馏等过程,可获得清洁能源和重要的化工原料 | |
| D. | 神舟10号飞船所用太阳能电池板可将光能转换为电能,所用转换材料是单晶硅 |

| A. | H2S是一种弱电解质 | |
| B. | 可用石灰乳吸收H2S气体 | |
| C. | 根据如图可知FeCl3、CuCl2均能氧化H2S | |
| D. | H2S在空气中燃烧可以生成SO2 |
| A. | 该溶液中氢离子的浓度:c(H+)=1×10-11 mol•L-1 | |
| B. | pH=7 的NH4Cl和NH3•H2O的混合溶液:c(Cl-)>c(NH4+)>c(H+)=c(OH-) | |
| C. | 浓度均为0.1 mol•L-1的NH3•H2O和NH4Cl溶液等体积混合后的碱性溶液中:c(NH4+)>c(Cl-)>c(NH3•H2O)>c(OH-)>c(H+) | |
| D. | 0.1 mol•L-1的氨水与0.05 mol•L-1的 H2SO4溶液等体积混合后所得溶液中:2c(NH4+)+2c(NH3•H2O)=c(SO42-) |

| A. | 溶液中一定不存在CO32- | B. | 溶液中一定不存在Fe3+ | ||
| C. | 溶液中一定存在K+ | D. | 溶液中c(NO3-)=0.1mol/L |
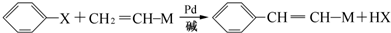
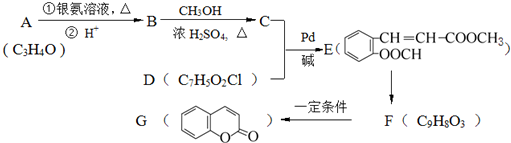

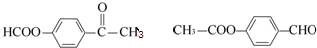
 )常用作香豆素的替代品.鉴别二氢香豆素和它的一种同分异构体(
)常用作香豆素的替代品.鉴别二氢香豆素和它的一种同分异构体( )需要用到的试剂有:NaOH溶液、稀硫酸、氯化铁溶液
)需要用到的试剂有:NaOH溶液、稀硫酸、氯化铁溶液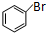 +CH2═CHCOOCH3$→_{碱}^{Pd}$
+CH2═CHCOOCH3$→_{碱}^{Pd}$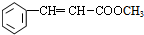 +HBr.
+HBr.