题目内容
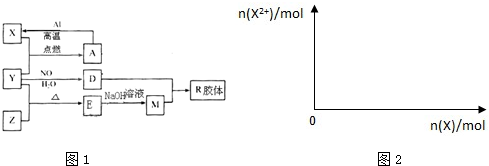
16. 三氯异氰尿酸是一种极强的氧化剂和氯化剂,利用氰尿酸(如图1)与次氯酸在一定pH下反应可制备三氯异氰尿酸(如图2),若原料完全反应生成三氯异氰尿酸.则氰尿酸和次氯酸的物质的量之比应为( )
三氯异氰尿酸是一种极强的氧化剂和氯化剂,利用氰尿酸(如图1)与次氯酸在一定pH下反应可制备三氯异氰尿酸(如图2),若原料完全反应生成三氯异氰尿酸.则氰尿酸和次氯酸的物质的量之比应为( )| A. | 1:1 | B. | 2:3 | C. | 1:2 | D. | 1:3 |
分析 氰尿酸与次氯酸在一定pH下发生取代反应可制备三氯异氰尿酸,反应方程式为: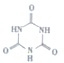 +3HOCl→
+3HOCl→ +3H2O,由此分析解答.
+3H2O,由此分析解答.
解答 解:氰尿酸与次氯酸在一定pH下发生取代反应可制备三氯异氰尿酸,反应方程式为: +3HOCl→
+3HOCl→ +3H2O,所以氰尿酸和次氯酸的物质的量之比应为1:3,故选D.
+3H2O,所以氰尿酸和次氯酸的物质的量之比应为1:3,故选D.
点评 本题以三氯异氰尿酸为载体,考查化学反应的特点和应用,注意次氯酸的结构和性质,以及取代反应的特点,难度不大.

练习册系列答案
相关题目
6.某研究性学习小组探究FeSO4的化学性质和用途.回答下列问题:
(一)探究FeSO4溶液的酸碱性:
取少量FeSO4固体,利用石蕊试液测试FeSO4溶液的酸碱性,必须选用的仪器有胶头滴管、药匙和B.
A.玻璃棒 B.试管 C.天平 D.量筒
(二)利用下图装置探究FeSO4的稳定性
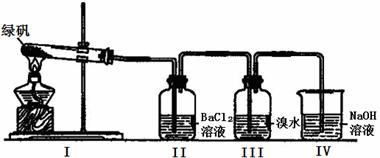
Ⅱ中有白色沉淀生成,小组成员结合理论分析,认为下列分解产物不可能的是A.
A.Fe2O3、SO3、H2O B.Fe2O3、SO2、SO3、H2O
C.FeO、Fe2O3、SO2、SO3、H2O
Ⅲ中溴水是用来检验是否有 SO2气体生成,若有SO2生成,溴水将褪色.实验中,观察到溴水褪色,据此推测FeSO4分解最有可能被氧化的元素是Fe.NaOH的作用是吸收SO2气体,请 写出最大量吸收SO2气体的反应化学方程式:2NaOH+SO2=Na2SO3+H2O.
(三)探究FeSO4中Fe2+还原性:
证明FeSO4有较强的还原性,完成下表.
(四)硫酸亚铁用途探究
缺铁性贫血往往口服硫酸亚铁,当用硫酸亚铁制成药片时,外表包有一层特殊的糖衣,其作用是防止硫酸亚铁被氧化.
(一)探究FeSO4溶液的酸碱性:
取少量FeSO4固体,利用石蕊试液测试FeSO4溶液的酸碱性,必须选用的仪器有胶头滴管、药匙和B.
A.玻璃棒 B.试管 C.天平 D.量筒
(二)利用下图装置探究FeSO4的稳定性

Ⅱ中有白色沉淀生成,小组成员结合理论分析,认为下列分解产物不可能的是A.
A.Fe2O3、SO3、H2O B.Fe2O3、SO2、SO3、H2O
C.FeO、Fe2O3、SO2、SO3、H2O
Ⅲ中溴水是用来检验是否有 SO2气体生成,若有SO2生成,溴水将褪色.实验中,观察到溴水褪色,据此推测FeSO4分解最有可能被氧化的元素是Fe.NaOH的作用是吸收SO2气体,请 写出最大量吸收SO2气体的反应化学方程式:2NaOH+SO2=Na2SO3+H2O.
(三)探究FeSO4中Fe2+还原性:
证明FeSO4有较强的还原性,完成下表.
| 实验步骤 | 实验预期现象及结论 |
| 步骤一:取少量的FeSO4 固体于试管中,加入一定量水溶解 | |
| 步骤二: |
缺铁性贫血往往口服硫酸亚铁,当用硫酸亚铁制成药片时,外表包有一层特殊的糖衣,其作用是防止硫酸亚铁被氧化.
4.装置(Ⅰ)为铁镍(Fe-Ni)可充电电池:Fe+NiO2$?_{充电}^{放电}$Fe(OH)2+Ni(OH)2;装置(Ⅱ)为电解示意图,当闭合开关K时,Y附近溶液先变红.下列说法正确的是( )
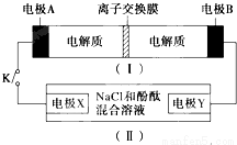

| A. | 闭合K时,X的电极反应式为:2H++2e-═H2↑ | |
| B. | 闭合K时,A电极反应式为:NiO2+2e-+2H+═Ni(OH)2 | |
| C. | 给装置(Ⅰ)充电时,B极参与反应的物质被氧化 | |
| D. | 给装置(Ⅰ)充电时,OH-通过阴离子交换膜,移向A电极 |
1.向AgNO3溶液中加入一定质量Fe和Al的混合溶液,充分反应后过滤,得到滤渣和浅绿色滤液.下列说法正确的是( )
| A. | 滤液中一定含有Al3+、Ag+ | B. | 滤液中一定含有Fe2+、Ag+ | ||
| C. | 滤渣中一定含有Fe | D. | 滤渣中一定含有Ag |
6.质量分数不等的两种硫酸钠溶液等质量混合时,其质量分数为a%,而等体积混合后的质量分数为b%;
质量分数不等的两种乙醇溶液等质量混合时,其质量分数为a%,而等体积混合后的质量分数为c%.则
a、b、c的大小关系正确的是( )
质量分数不等的两种乙醇溶液等质量混合时,其质量分数为a%,而等体积混合后的质量分数为c%.则
a、b、c的大小关系正确的是( )
| A. | a>b>c | B. | b>a>c | C. | c>a>b | D. | c>a>b |
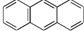 与苯炔
与苯炔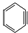 反应生成化合物X(立体对称图形),如图所示:
反应生成化合物X(立体对称图形),如图所示: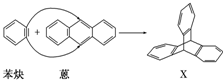
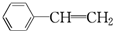 B.
B.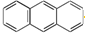 C.
C.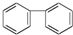 D.
D.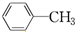
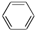 B.C6H14 C.
B.C6H14 C.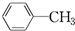 D.
D.
 .
.