【题目】某校研究性学习小组在探究中和反应时,先取10mL稀氢氧化钠溶液,滴加两滴酚酞溶液,溶液显红色。然后逐滴滴入稀盐酸并搅拌,至红色恰好变成无色。小组同学对该实验进行了如下探究:
(1)请写出氢氧化钠溶液和盐酸反应的化学方程式_____。
(2)深入探究:上述反应中, 究竟是稀盐酸中哪种粒子参加反应?
[提出假设]假设1: H2O 参加反应;
假设2: H+ 参加反应;
假设3:_____参加反应
[设计实验]
学习小组的同学们取10mL稀氢氧化钠溶液,滴加两滴酚酞溶液,将变红后的溶液分成四等分后分别置于四支试管中,进行如下实验:
实验编号 | 实验步骤 | 实验现象 | 结论 |
① | 向其中一支试管滴加1mL蒸馏水 | 溶液不变色 | 假设1不成立 |
② | 向其中一支试管滴加1mL稀硫酸溶液 | 溶液变成无色 | 假设2_____(填“成立”或“不成立”) |
向其中一支试管滴加1mL硫酸钠溶液 | 溶液不变色 | ||
③ | 向其中一支试管滴加1mL_____溶液 | 溶液不变色 | 假设3_____(填“成立”或“不成立”) |
[实验反思]
经过讨论,小组同学一致认为假设1不需要经过实验就可以推导出其不成立,理由是_____。
[实验拓展]小琳同学查阅资料后发现,对于没有明显现象的化学变化,可以通过验证反应物消失、新物质生成、监测温度、pH变化等来“造出现象”,使反应现象明显,从而获得正确的认识。请再设计出一种不同的实验方案证明氢氧化钠溶液与稀盐酸确实发生了化学反应:_____。
[实验延伸]小芳同学实验后与同组其他同学认真讨论,然后认为直接向含有酚酞溶液的氢氧化钠溶液中滴加稀盐酸,观察到红色褪去,并不能证明就是加入的稀盐酸与氢氧化钠发生反应,你认为她的观点是否合理?并说明理由。_____。
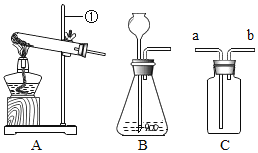
【题目】在学习“燃烧与灭火”的课堂上,老师做了一个有趣的实验:将一根铜丝绕成线圈,罩在蜡烛火焰上(如图所示),观察到火焰立即熄灭。

(1)探究一:蜡烛熄灭的原因。
猜想与假设: a.铜线圈隔离了可燃物:
b.铜线圈隔绝了空气;
c.铜线圈吸热,降温至蜡烛着火点以下。
讨论与交流:经观察分析同学们否定了猜想a和b,理由是_____。
设计并进行如下实验:
实验操作 | 实验现象 | 结论 |
将铜圈加热后_____ | _____ | 猜想c正确 |
(2)探究二:经过多次上述实验,大家发现铜丝表面变黑,黑色物质是什么呢?
猜想与假设:①炭黑;②_____; ③炭黑和氧化铜。
讨论交流:铜丝表面产生炭黑的原因是_____。
实验操作 | 实验现象 | 结论 |
取少许黑色固体至试管中,_____ | _____ | 猜想③正确 |