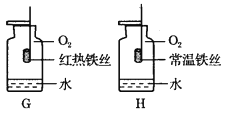
题目内容
【题目】回答下列问题。
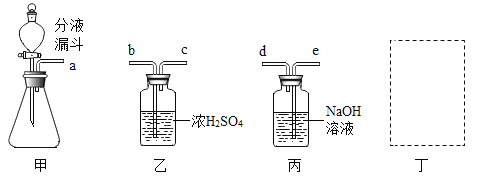
(1)![]() 、
、![]() 、
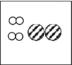
、![]() 分别表示氧元素的三种原子,可简写成16O、17O、18O。18O 在化学原理探究和核化学方面有广泛应用。电解重氧水(H2 18O)可以获得重氧(18O 2),请据下图回答:
分别表示氧元素的三种原子,可简写成16O、17O、18O。18O 在化学原理探究和核化学方面有广泛应用。电解重氧水(H2 18O)可以获得重氧(18O 2),请据下图回答:

①16O、17O、18O 三种原子中, ________________数目相等(填“质子”“中子”或“电子”)。
②H2 与 18O2 反应生成的水可表示为 H2 18O。写出电解H218O反应的化学方程式____________ ,在图中的小方框中,把电解 H218O 恰好完全反应的生成物微观粒子补画齐全___________。
(2)2017年,哈佛大学科学家将微小的固态氢置于488万个大气压下,氢气分子破裂为氢原子,由氢原子 直接构成金属氢。金属氢具有金属的性质,储藏着巨大的能量。氢气和金属氢性质 _________(填“相同” 或“不同)。
(3) 科学家用氙气(Xe)和PtF6合成了化合物XePtF6,其中PtF6为带一个单位负电荷的根离子,则氙离子 的化学符号为________,XePtF6中Pt元素的化合价为_______。
(4) 鱼头汤的鲜味主要来源于鱼头中的____________ ,在煨煮过程中转化生成的氨基酸。
(5) 尿素与二氧化氮反应可以消除二氧化氮的污染,该反应的化学方程式为:4CO(NH2)2+6NO2 4CO2+8H2O+X。X的内容为_________________________。
4CO2+8H2O+X。X的内容为_________________________。
【答案】质子、电子 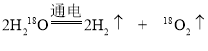
 不同
不同 ![]() +5 蛋白质
+5 蛋白质 ![]()
【解析】
(1)在元素周期表中原子的原子序数等于质子数也等于核外电子数,16O、17O、18O 三种原子中,原子序数相同,那么质子数相同,电子数也相同;质量数=质子数+中子数,三种原子中质量数不相同,那么中子数也不相同,所以16O、17O、18O 三种原子中质子、电子数目相等。电解H218O反应的化学方程式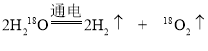 ,根据化学方程式分析,图中的小方框中的生成物微观粒子还差一个重氧分子,补画齐全如图:
,根据化学方程式分析,图中的小方框中的生成物微观粒子还差一个重氧分子,补画齐全如图: 。
。
(2)氢气是由氢分子构成的,而金属氢是由氢原子直接构成的。两种物质的构成不同,性质就不同,所以氢气和金属氢性质不同。
(3)在化合物正负电荷电量相等,电性相反,在XePtF6中PtF6为带一个单位负电荷的根离子,那么氙离子就带一个单位的正电荷,化学符号为![]() ,在XePtF6中Xe元素的化合价为+1,F元素的化合价为-1,根据化合物中正负化合价代数和为0,设Pt元素的化合价为X,则
,在XePtF6中Xe元素的化合价为+1,F元素的化合价为-1,根据化合物中正负化合价代数和为0,设Pt元素的化合价为X,则![]() ,解得X=+5。
,解得X=+5。
(4)鱼肉中富含蛋白质,蛋白质在煨煮过程中转化生成氨基酸。
(5)根据反应元素种类不变,对化学方程式4CO(NH2)2+6NO2 4CO2+8H2O+X进行微观分析,反应前后C、O、H原子个数相等,X中一定不含C、O、H原子,反应前N原子个数为14,反应后二氧化碳和水不含氮原子,则X是由氮原子构成的单质分子,且X中共有14个氮原子,符号为:
4CO2+8H2O+X进行微观分析,反应前后C、O、H原子个数相等,X中一定不含C、O、H原子,反应前N原子个数为14,反应后二氧化碳和水不含氮原子,则X是由氮原子构成的单质分子,且X中共有14个氮原子,符号为:![]() 。
。

【题目】某化学兴趣小组为了测定粗锌中锌的质量分数,在10g粗锌中分5次共加入50.0g稀硫酸(杂质不与硫酸反应),部分数据如下表所示,请计算:
容器中硫酸的质量/g | 10 | 20 | 40 | 50 |
气体质量/g | 0.1 | 0.2 | m | 0.3 |
(1)当加入40g硫酸时,对应的气体质量m是___________g。
(2)粗锌中锌的质量_______________________。
【题目】在学习“燃烧与灭火”的课堂上,老师做了一个有趣的实验:将一根铜丝绕成线圈,罩在蜡烛火焰上(如图所示),观察到火焰立即熄灭。

(1)探究一:蜡烛熄灭的原因。
猜想与假设: a.铜线圈隔离了可燃物:
b.铜线圈隔绝了空气;
c.铜线圈吸热,降温至蜡烛着火点以下。
讨论与交流:经观察分析同学们否定了猜想a和b,理由是_____。
设计并进行如下实验:
实验操作 | 实验现象 | 结论 |
将铜圈加热后_____ | _____ | 猜想c正确 |
(2)探究二:经过多次上述实验,大家发现铜丝表面变黑,黑色物质是什么呢?
猜想与假设:①炭黑;②_____; ③炭黑和氧化铜。
讨论交流:铜丝表面产生炭黑的原因是_____。
实验操作 | 实验现象 | 结论 |
取少许黑色固体至试管中,_____ | _____ | 猜想③正确 |