题目内容
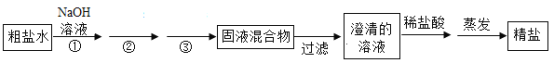
【题目】近十年来,随着生活水平的提高,电瓶车已经走入千家万户,极大方便民众日常出行的同时,废旧电瓶车如何处理显得越来越重要。我校研究性学习小组欲从某废弃电瓶车的电池(主要含有LiMn2O4和碳粉)中提取二氧化锰,其部分工艺流程如图:
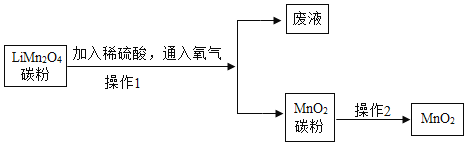
(1) MnO2 中锰的化合价是_____。
(2)操作1中需要使用玻璃棒,其作用是_____,废液中一定含有的金属元素是_____。(写名称)。
(3)操作2的名称是_____,写出该操作中发生的主要反应的化学方程式_____。
(4)你认为回收废旧电瓶车有何意义?_____(写一点即可)。
【答案】+4 引流 锂 灼烧 ![]()
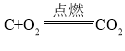 收回资源,减少污染(合理即可)
收回资源,减少污染(合理即可)
【解析】
(1)MnO2中氧元素为-2价,根据化合物中正负化合价的代数和为零可得,设锰的化合价为x,则:x+(-2)×2=0,得x=+4。
(2)操作1实现固体和液体分离,为过滤,此过程中玻璃棒的作用是引流。由于是某废弃电瓶车的电池(主要含有LiMn2O4和碳粉)和硫酸以及氧气反应得到二氧化锰和碳以及废液,根据质量守恒定律可知,锂元素一定在废液中。所以废液中一定含有的金属元素的名称是锂。
(3)操作2是在空气中灼烧混合物,使碳转化为二氧化碳而得到纯净的二氧化锰,所以操作2名称是灼烧,该操作中发生的主要反应的化学方程式 C+O2![]() CO2。
CO2。
(4)你认为回收废旧电瓶车 意义:收回资源,减少污染(写一点即可)
故答案为:
(1)+4。
(2)引流;锂。
(3)灼烧; C+O2![]() CO2。
CO2。
(4)收回资源,减少污染。

练习册系列答案
相关题目