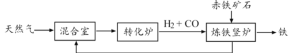
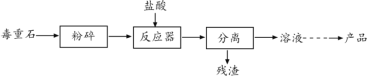
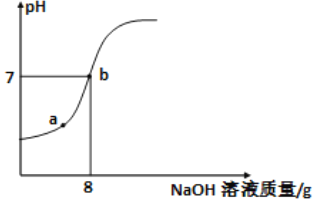
【题目】某小组同学通过资料发现,向不同浓度的碳酸钠和碳酸氢钠溶液中加入氯化钙溶液,会出现以下现象。继而对氯化钙与两种溶液的反应进行了探究。
Na2CO3 | NaHCO3 | |
现象一 | 产生沉淀 | 产生沉淀和气泡 |
现象二 | 产生沉淀 | 产生沉淀 |
现象三 | 产生沉淀 | 无沉淀 |
(查阅资料)
①![]()
②Ca(HCO3)2易溶于水。
(进行实验)
实验一:70℃恒温水浴下,向10 mL不同浓度的Na2CO3和NaHCO3溶液中滴加10%的CaCl2溶液,现象如下表。
浓度 | Na2CO3 | NaHCO3 |
10% | 滴加1滴出现白色沉淀 | 滴加1滴出现白色沉淀,有较多气泡产生 |
5% | 滴加1滴出现白色沉淀 | 滴加1滴出现白色沉淀,30 s后有少量气泡产生 |
1% | 滴加1滴出现白色沉淀 | 滴加10滴出现浑浊 |
0.5% | 滴加1滴出现白色沉淀 | 滴加52滴出现浑浊 |
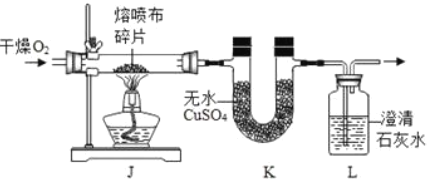
实验二:如图进行实验。70℃恒温水浴下,向10 mL不同浓度的NaHCO3溶液中滴加10%的CaCl2溶液,测得CO2浓度与时间的关系如下图。

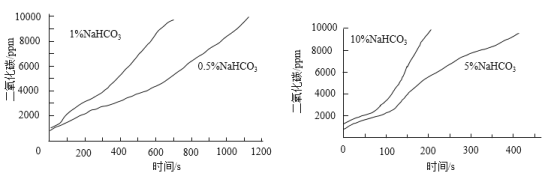
(解释与结论)
(1)NaHCO3的俗称是________。
(2)![]() 属于基本反应类型中的________反应。
属于基本反应类型中的________反应。
(3)补全NaHCO3与CaCl2反应的化学方程式:![]() +________+________+H2O。
+________+________+H2O。
(4)实验二得出的结论是________。
(反思与评价)
(5)实验一中,向NaHCO3溶液中滴加CaCl2溶液时,有些只观察到浑浊、未观察到气泡,原因可能是________。
(6)小组同学发现的资料,现象三的NaHCO3溶液中无沉淀,其原因可能为_______。
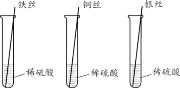
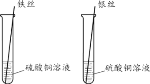
【题目】证明铁、铜、银金属活动性。请选择一种方案作答,若均作答,按第一个计分。
方案一 | 方案二 |
|
|
(1)发生反应的化学方程式为______。 | (1)发生反应的化学方程式为______。 |
(2)能否实现目的及原因分别是______。 | (2)观察到的现象是______。 |
【题目】下表是几种家用清洁剂。
清洁剂 | 洁厕灵 | 彩漂液 | 管道通 |
功能 | 清除污垢 | 使衣物色彩鲜艳 | 管道疏通 |
有效成分 | HCl | H2O2 | NaOH |
(1)三种清洁剂的有效成分,相对分子质量为34的是______。
(2)管道通在使用时禁止与皮肤接触,其原因是______。
(3)洁厕灵可以去除铁管表面的锈迹,用化学方程式表示其原因是______。
【题目】A B C D表示4种物质,其微观示意图见下表,A和B在一定条件下反应生成C和D。下列说法不正确的是
物质 | A | B | C | D |
|
微观示 意图 |
|
|
|
|
A.B的化学式为SO2
B.生成的C为单质
C.参加反应的A和B分子个数比为2:1
D.16gB参加反应,则生成C的质量为8g
【题目】阅读下面科普短文。
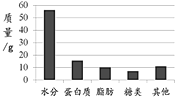
腐乳是中华民族独特的传统调味品,具有悠久的历史。它是一种微生物发酵大豆制品,营养成分(以100g计)如图。腐乳营养价值与奶酪相当,具有东方奶酪之称。
腐乳发酵分为前期发酵和后期发酵,其制作工序大致如下:
![]()
前期发酵主要是培养毛霉菌的过程,毛霉生长的好坏将决定着腐乳最终的质量。影响毛霉生长的因素主要有温度、湿度、培养时间等。
实验:将豆腐坯在湿度为95%下进行前期发酵,观察毛霉生长状况。
时间/h | 24 | 36 | 48 | 54 | |
温度 | 15℃ | 无菌丝 | 有菌丝,较细 | 菌丝密集、较粗壮、较白 | 菌丝出现老化,稍变灰 |
25℃ | 有菌丝,较细 | 菌丝浓密、粗壮、银白色 | 菌丝浓密、粗壮、银白色 | 少数菌丝出现老化,开始变灰 | |
30℃ | 长满菌丝,细长 | 菌丝浓密、粗壮、银白色 | 菌丝大多数老化,开始变灰黑 | 菌丝基本都老化,变黑 | |
后期发酵是在前期发酵的基础上加入食盐、红曲、黄酒等辅料,装坛后经过复杂的生物化学变化,将蛋白质分解为多肽和氨基酸等物质,腐乳特殊的色、香、味主要是在这个阶段形成的。(原文作者王鋆、张岭、刘景春等,有删改)
依据文章内容,回答下列问题。
(1)除水外,腐乳中营养成分含量最高的是______。
(2)腐乳中含有丰富的钙和磷,钙和磷指的是______(填“单质”或“元素”)。
(3)腐乳具有东方奶酪之称的原因是______。
(4)将蛋白质分解为多肽和氨基酸等物质的过程属于______变化。
(5)以下说法正确的是______(填序号)。
A温度和时间均影响毛霉生长
B在实验的温度下,15℃最适宜毛霉生长
C时间越长毛霉生长越好
D加盐腌坯中加的“盐”指的是食盐
【题目】敞口放置于空气中的氢氧化钠溶液能够发生下列变化而变质:

上述反应①的化学方程式为_____________, NaHCO3俗称______。某校化学学习小组师生对一瓶氢氧化钠溶液的变质情况进行了如下探究:
(提出问题)NaOH是否变质?
(做出猜想)
猜想1:NaOH全部变质。
猜想2:_____
(制定计划)老师探究是否产生了NaHCO3,学生在老师探究的基础上进一步探究。
(进行试验)
试验操作 | 试验现象 | 试验分析 | |
老师试验 | 略 | 略 | 没有产生NaHCO3 |
学生试验 | a,取一定量的待测液于试管中,加入足量CaCl2溶液 | 产生白色沉淀 | 反应的化学方程式为______ |
b,充分反应后静置,取上层清液加入无色酚酞溶液 | 溶液变红 | 原待测液中含有______ |
(表达交流)有同学认为上述实验a中的CaCl2溶液可改为澄清石灰水,你是否同意这种看法?_____(填“同意”或“不同意”)。
(实验结论)上述猜想2成立。
(反思评价)在实验室中,氢氧化钠应密封保存。