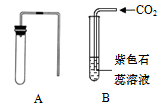
【题目】氢氧化钠和氢氧化钙是两种常见的碱。甲同学将两种碱的溶液分别装入试管A、B,并进行了如下图所示的二组实验。
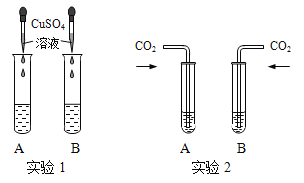
①实验1中,若B中是NaOH溶液,滴加硫酸铜溶液静置后得到蓝色不溶物和无色清液,则清液中溶质的成分是 (13) (用化学式表示)。
②实验2中,甲同学向两支试管中分别通入适量的二氧化碳,A(氢氧化钙溶液)中有白色沉淀生成,发生反应的化学方程式为 (14) ,B(氢氧化钠溶液)中无明显现象。
 ③为了探究实验2中二氧化碳是否与氢氧化钠反应,甲同学又设计了如下对比实验:
③为了探究实验2中二氧化碳是否与氢氧化钠反应,甲同学又设计了如下对比实验:
乙同学认为该实验设计不符合对比实验的基本 原则,理由是 (15) 。 |
④为了探究实验2中B中溶质的成分,丙同学进行了如下探究:
【提出猜想】猜想1:溶质只有氢氧化钠
猜想2:溶质只有碳酸钠
猜想3:溶质有氢氧化钠和碳酸钠
【实验探究】
实 验 操 作 | 实验现象 | 结 论 |
I.取B中少量溶液于试管中,加入足量澄清石灰水。 II.静置后,取上层清液,向其中加几滴酚酞试液。 | (16) | 猜想3成立 |
【反思与评价】
老师评价丙同学得出的结论不正确,原因是 (17) ;
为了使“猜想3成立”,丙同学对上述“实验探究”进行了改动,他的做法是 (18) 。
【题目】下表是KCl和KNO3在不同温度下的溶解度。
温度 / ℃ | 20 | 30 | 40 | 50 | |
溶解度(g/100g水) | KCl | 34.0 | 37.0 | 40.0 | 42.6 |
KNO3 | 31.6 | 45.8 | 63.9 | 85.5 | |
①硝酸钾的溶解度随温度的升高而 (7) (填“增大”或“减小”)。
②用同一种方法可以使KCl、KNO3二种物质的溶液都析出晶体,该方法是 (8) 。
③ KCl、KNO3两种物质溶解度相等的温度在 (9) 之间(用编号表示)
A.20℃以下 B.20℃~30℃ C.30℃~40℃ D.40℃~50℃
④20℃时,100g水中最多可溶解KCl (10) g;40℃时,将70g KCl的饱和溶液稀释成质量分数为20%的溶液,需加水 (11) g。
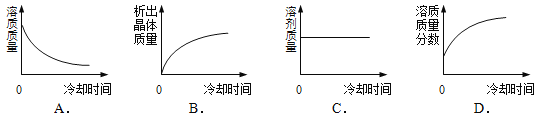
⑤将某温度下热的硝酸钾饱和溶液逐渐冷却至室温,下列有关量随时间变化趋势的图像不正确的是 (12) (用编号表示)
⑥实验设计:将不饱和氯化钾溶液变为饱和溶液
实验步骤 | 实验现象 | 实验结论 |
向不饱和的氯化钾溶液 中不断加入氯化钾固体 | (13) | KCl不饱和溶液 变为饱和溶液 |