题目内容
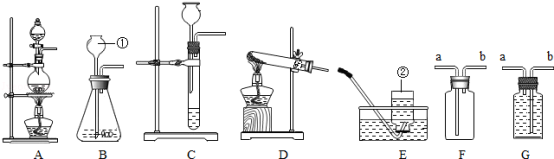
【题目】下图是实验室制取气体的一些装置,据图回答有关问题。
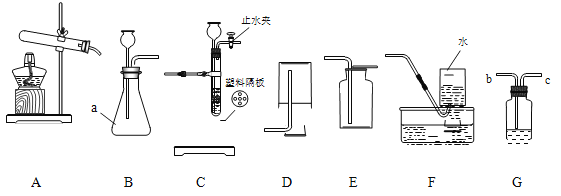
①仪器a的名称是 (3) 。
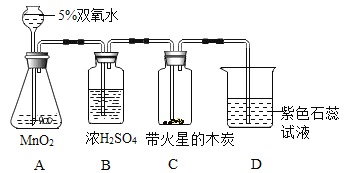
②实验室用过氧化氢溶液和二氧化锰粉末制氧气,可选用的发生装置是 (4) (填编号);收集氧气可选用E或F装置,由此推断氧气具有的物理性质是 (5) 。
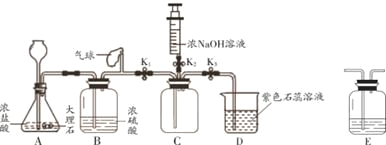
③实验室常用稀盐酸与石灰石反应制取二氧化碳气体:
I.该反应的化学方程式为 (6) 。
II.甲同学选择B装置为发生装置,使用长颈漏斗的目的是 (7) ;乙同学选择C装置为发生装置,一段时间后不再有气泡产生,在解释“不再有气泡产生”的原因时,乙同学认为可能是石灰石与稀盐酸脱离了接触,你认为还可能的原因是 (8) 。
III.用装置E收集二氧化碳,检验气体收集满的方法是 (9) 。
IV.该反应生成的二氧化碳中常混有少量氯化氢气体,某同学想通过装置G探究是否有HCl气体,你认为G中盛放的试剂是 (10) ,混合气体应从 (11) (填“b”或“c”)进入。
④通过对实验室制取气体的学习,你认为实验室制取气体的反应,共同点是 (12) (填序号)。
A.需要加热 B.反应物中没有气体参加
C.需要催化剂 D.反应物中必须含有要制取物质的元素
【答案】(3)锥形瓶(4)B(5)氧气密度比空气大,不易溶于水(6)CaCO3+2HCl→CaCl2+H2O+CO2↑(7)方便添加液体(8)可能是某种反应物已经消耗完毕(9)用燃着的木条放在瓶口,熄灭则集满(10)硝酸银溶液(11)b④(12)BD
【解析】
试题分析:实验室用过氧化氢溶液和二氧化锰粉末制氧气,反应不需要加热,故选B装置,装置E用向上排空气法收集气体,所以可说明氧气的密度比空气大,装置F是用排水法收集气体,说明氧气的不易溶于水,故氧气具有的性质的密度比空气大,不易溶于水实验室用稀盐酸与石灰石反应生成氯化钙,水和二氧化碳来制取二氧化碳,反应化学方程式为CaCO3+2HCl→CaCl2+H2O+CO2↑; 使用长颈漏斗的目的是方便添加液体,更好的控制反应的进行,反应会生成二氧化碳气体,装置中会有气泡的产生,此时不再有气泡产生,可能是石灰石与稀盐酸脱离了接触使反应不能进行,还有可能是某种反应物已消耗完毕,也终止了反应,不会有气泡的产生; 检验二氧化碳是否收集满的方法是用燃着的木条放在瓶口,燃着的木条熄灭则表示已集满;探究是否含有HCl气体,通常用硝酸银检验,如果混有则G中会产生白色沉淀,反之则不混有,混合气体应从导管b进入,使二氧化碳和硝酸银充分接触,更好的除去HCl气体 ④实验室制取气体的反应,共同点是反应物中没有气体参加反应,并且反应物中必须含有要制取物质的元素,BD项正确,氯酸钾制氧气不需要催化剂,过氧化氢制氧气不需要加热,故加热和需要催化剂不是共同点,故AC项错误。