题目内容
【题目】某未知溶液X,溶质可能是硫酸、碳酸钾、氯化镁中的一种或两种。为确定溶质成分,进行下列探究活动:

(提出问题)X溶液中的溶质是什么?
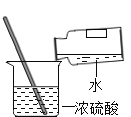
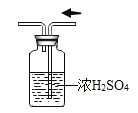
(实验探究)根据可能存在的溶质的性质,石建设计并进行实验。
(收集证据)根据B中现象,石建判断A中发生反应的化学方程式为(1)_______,得出X溶液中的溶质只有硫酸的结论。
(表达交流)秦思对石建的实验及得出结论的可靠性提出质疑,理由是(2)_______。
(解释结论)经过讨论,小组同学认同秦思的理由,针对石建实验存在的问题,在其实验的基础上进行改进,继续探究,如上图所示。D—F观察到(3)_____________,
据此确定石建的结论错误,最终确定了溶液中溶质的成分。通过对B、D白色固体成分的比较,并结合此实验整个过程中观察到的现象,你还能推断出的结论是(4)_______
(问题处理)如何实现废液的绿色排放?
(查阅资料)钡离子有毒
(问题解决)通过对E、F溶质成分的判断,裘臻将E、F溶液混合,若混合后废液恰好符合排放标准,最终排放的液体中一定含有的离子是(5)___________(填符号)。
(归纳总结)经历上述探究过程,可以总结出:探究溶液中溶质的成分时,当所加试剂与溶液中可能存在的两种及两种以上的溶质(或离子)都能发生反应且产生相同的现象时,要考虑(6)_____ 。确定溶质的思路是:根据实验事实与证据可确定(7) ___________,并据其确定_________。
【答案】Ba(OH)2+H2SO4=BaSO4↓+2H2O 硫酸、碳酸钾、氯化镁三种物质中滴加氢氧化钡时,硫酸先反应,碳酸钾、氯化镁后反应; 固体部分溶解 溶液中一定不含碳酸钾 Cl-和Mg2+ 生成物性质的不同 一定存在的物质 与已证明存在的物质不共存的物质一定不存在
【解析】
[收集证据]硫酸与氢氧化钡生成硫酸钡沉淀、碳酸钾和氢氧化钡生成硫酸钡沉淀,碳酸钡沉淀溶于硝酸,而硫酸钡沉淀不溶于硝酸,氯化镁和氢氧化钡生成氯化钡和氢氧化镁沉淀,氢氧化镁沉淀溶于硝酸,根据B中沉淀中加足量硝酸,固体无变化现象,石建判断A中一定有硫酸,没有氯化镁和碳酸钾,发生反应的化学方程式为Ba(OH)2+H2SO4=BaSO4↓+2H2O;
[表达交流]秦思对石建的实验及得出结论的可靠性提出质疑,理由是硫酸、碳酸钾、氯化镁三种物质中滴加氢氧化钡时,硫酸先反应,剩余的氢氧化钡才与氯化镁、碳酸钾反应,而实验中滴入少量氢氧化钡,可能导致氢氧化钡都被硫酸反应,与氯化镁、碳酸钾反应有没发生;
[解释结论]经过讨论,小组同学认同秦思的理由,针对石建实验存在的问题,在其实验的基础上进行改进,继续探究,如上图所示。D—F观察到固体部分溶解,证明溶液中有氯化镁;据此确定石建的结论错误。通过对B、D白色固体成分的比较,并结合此实验整个过程中观察到的现象,还能推断出的结论是溶液中一定不含碳酸钾,因硫酸和碳酸钾不共存;
[问题解决]E溶液中有生成的氯化钡和过量的氢氧化钡、F溶液中有过量的硫酸和生成的硫酸镁,裘臻将E、F溶液混合,若混合后废液恰好符合排放标准,说明硫酸和氯化钡、氢氧化钡刚好完全反应,溶液中只有溶质氯化镁,最终排放的液体中一定含有的离子是氯离子Cl-和镁离子Mg2+;
[归纳总结]经历上述探究过程,可以总结出:探究溶液中溶质的成分时,当所加试剂与溶液中可能存在的两种及两种以上的溶质(或离子)都能发生反应且产生相同的现象时,要考虑生成物的性质的区别。确定溶质的思路是:根据实验事实与证据可确定一定存在的物质,并据其确定与证明存在的物质不共存的物质一定不存在。

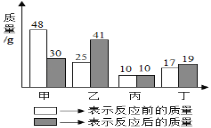
【题目】下列四个图象中,能正确反映对应变化关系的是( )
|
|
|
|
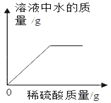
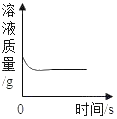
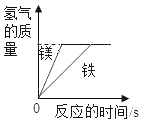
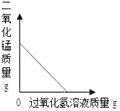
A.向一定质量的氢氧化钠溶液中加入稀硫酸至过量 | B.向一定质量的稀硫酸中加入锌片 | C.常温下,足量的镁、铁分别同时放入少量等质量、等质量分数的稀盐酸中 | D.向一定质量的二氧化锰中加入过氧化氢溶液 |
A. AB. BC. CD. D
【题目】小王同学为了测定某Na2CO3溶液中溶质的质量分数,取10g该溶液于烧杯中,然后将400g澄清石灰水分四次加入,烧杯中沉淀的质量与每次加入澄清石灰水的质量关系如表。请计算:
第一次 | 第二次 | 第三次 | 第四次 | |
加入澄清石灰水的质量/g | 100 | 100 | 100 | 100 |
生成沉淀的质量/g | 0.4 | m | 1.0 | 1.0 |
(1)表中m的值为_____。
(2)Na2CO3溶液中溶质的质量分数_____(写出计算过程)。