题目内容
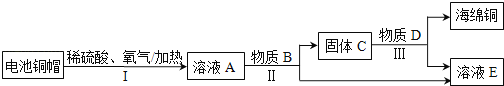
【题目】中国芯彰显中国“智”造,芯片的基材主要是高纯硅(Si),下图是某种制备高纯硅的工艺流程图:
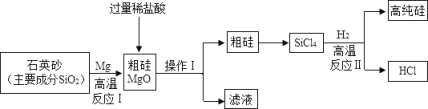
(1)地壳中硅元素的含量比铝_____(填“高”或“低”),二氧化硅中硅元素化合价为_____。
(2)反应Ⅱ的化学方程式为____,该反应要在无氧环境中进行,原因是______(答出一种即可)。
(3)操作Ⅰ的名称是_____,所得粗硅应充分洗涤,以除去表面可能含有的盐酸、_____(填化学式)。
【答案】高; +4 ; 2H2+SiCl4![]() Si+4HCl ; 防止H2与O2 混合,高温时爆炸或生成的硅又被氧化; 过滤 ; MgCl2
Si+4HCl ; 防止H2与O2 混合,高温时爆炸或生成的硅又被氧化; 过滤 ; MgCl2
【解析】
(1)地壳中元素含量前五位依次是:氧、硅、铝、铁、钙,故硅元素含量比铝高;氧元素显-2价,设硅元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:x+(-2)×2=0,则x=+4.
(2)由图知,反应Ⅱ是SiCl4和H2反应生成Si和HCl,化学方程式为2H2+SiCl4![]() Si+4HCl;反应Ⅱ中涉及到易燃易爆的氢气,所以要在无氧气环境中进行,原因是防止H2与O2 混合,高温时爆炸或生成的硅又被氧化。
Si+4HCl;反应Ⅱ中涉及到易燃易爆的氢气,所以要在无氧气环境中进行,原因是防止H2与O2 混合,高温时爆炸或生成的硅又被氧化。
(3)操作Ⅰ实现固体和液体分离,为过滤;所得粗硅应充分洗涤,以除去表面可能含有的盐酸、MgCl2。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
【题目】KNO3的溶解度如表,下列说法错误的是
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
溶解度/g | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
A. 硝酸钾的溶解度受温度影响变化较大
B. 60 ℃时,饱和硝酸钾溶液中溶质与溶液质量之比为11∶21
C. 20 ℃时,10 g水中加入5 g硝酸钾充分溶解后再加入5 g水,前后溶质的质量分数不变
D. 将溶质质量分数为28%的硝酸钾溶液从60 ℃降温至20 ℃,没有晶体析出