题目内容
【题目】KNO3的溶解度如表,下列说法错误的是
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
溶解度/g | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
A. 硝酸钾的溶解度受温度影响变化较大
B. 60 ℃时,饱和硝酸钾溶液中溶质与溶液质量之比为11∶21
C. 20 ℃时,10 g水中加入5 g硝酸钾充分溶解后再加入5 g水,前后溶质的质量分数不变
D. 将溶质质量分数为28%的硝酸钾溶液从60 ℃降温至20 ℃,没有晶体析出
【答案】D
【解析】
A、从表格可以看出,硝酸钾的溶解度随温度的升高而增大,说法正确,不符合题意;
B、60℃时,硝酸钾的溶解度为110g,因此饱和硝酸钾溶液中溶质为110g,对应的溶剂就是100,则溶液为210g,因此溶质和溶液的质量比为100g:210g=11:21,说法正确,故不符合题意;
C、20℃时,硝酸钾的溶解度是31.6g,因此10g水中加入5g硝酸钾充分溶解只能溶解3.16g,再加入5g水,可以继续溶解1.58g的硝酸钾,形成的溶液仍然是此温度下的饱和溶液,因此溶质质量分数不变,说法正确,故不符合题意;
D、某温度下饱和溶液的![]() ,因此20℃时饱和的硝酸钾溶液中溶质质量分数为:
,因此20℃时饱和的硝酸钾溶液中溶质质量分数为:![]() ,因此会有晶体的析出,说法错误,故符合题意。
,因此会有晶体的析出,说法错误,故符合题意。
故选D。

 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案【题目】为了测定实验室某生锈铁片中铁元素的质量分数,两位同学分别设计了如下甲、乙两个实验方案。方案甲:称得生锈铁片的质量为 m1g,按图 I 所示装置进行实验。完全反应后,测得室温下产生氢气的体积为 V1L,查得其密度为p1g/L。方案乙:称得生锈铁片的质量为 m2g,先按图Ⅱ所示装置进行实验。当生锈铁片完全变成光亮的银白色时,停止加热,继续通入CO至室温。取出铁片,按图 I 所示装置继续进行实验。完全反应后,测得室温下产生氢气的体积为 V2L,查得其密度为 p2g/L。
已知:Fe2O3+6HCl=2FeCl3+3H2O(FeCl3可溶于水)
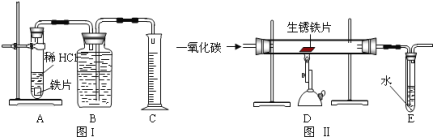
(1)铁锈的成分是__________.
(2)(评价交流)上述两个方案中,可行的是____(填“甲”或“乙”);分析不可行方案,其缺陷是____________________。
(3)(设计实验)方案乙中,同学们设计了如下实验报告,请帮助完成表中空格。
实验编号 | 实验步骤 | 实验现象 | 结论或化学方程式 |
①装置Ⅱ | 通入CO,加热.完全反应后,停止加热,继续通CO至室温 | 生锈铁片变成光亮的银白色 | CO具有______性; 化学方程式:_______ |
②装置Ⅰ | 将光亮铁片放入稀盐酸中,完全反应 | ______ |
(4)图Ⅱ所示装置有缺陷,应如何改进__________。
(5)(结论)生锈铁片中铁元素的质量分数是_________(用字母表示)。
(6)(发散)实验室经常用一氧化碳来炼铁,实验室炼的铁和工业炼的铁本质区别是_______________