题目内容
【题目】已知A是一种碱溶液,B是一种盐溶液。如图实验操作(每一步恰好完全反应,“↓”表示形成不溶于水的固体物质)
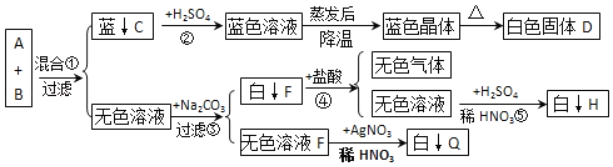
(1)根据如图实验操作写出下列物质的化学式:
A_____ B_____ C_____ Q_____。
(2)写出下列反应的化学方程式。②_____,⑤_____。
【答案】Ba(OH)2 CuCl2 Cu(OH)2 AgCl; Cu(OH)2+H2SO4=CuSO4+2H2O; BaCl2+H2SO4=BaSO4+2HCl
【解析】
A是一种碱溶液,B是一种盐溶液,且A+B→C蓝↓,C为蓝↓是该题的一个突破口,C一定就是Cu(OH)2;由此可知B中一定含有铜元素,C+H2SO4→蓝色溶液(CuSO4溶液)![]() 白色D,所以D就是CuSO4;有图示反应关系可知,H为不溶于酸的白色沉淀,是无色溶液与硫酸反应生成的,故H就是硫酸钡,即可知F就为碳酸钡,也可推知A中含有钡离子,则A就是氢氧化钡;无色溶液E+硝酸银和稀硝酸生白色沉淀Q,说明Q为不溶于酸的氯化银沉淀,及E中含有氯离子,有此可得B中含有氯离子,即B就是氯化钡,则E就是氯化钠。
白色D,所以D就是CuSO4;有图示反应关系可知,H为不溶于酸的白色沉淀,是无色溶液与硫酸反应生成的,故H就是硫酸钡,即可知F就为碳酸钡,也可推知A中含有钡离子,则A就是氢氧化钡;无色溶液E+硝酸银和稀硝酸生白色沉淀Q,说明Q为不溶于酸的氯化银沉淀,及E中含有氯离子,有此可得B中含有氯离子,即B就是氯化钡,则E就是氯化钠。
(1)由分析知A、B、C、Q的化学式为A:Ba(OH)2; B:CuCl2; C:Cu(OH)2; Q:AgCl;
(2)②是氢氧化铜和硫酸的反应,方程式为:Cu(OH)2+H2SO4=CuSO4+2H2O;③是氯化钡和硫酸反应,方程式为:BaCl2+H2SO4=BaSO4↓+2HCl。

【题目】为了测定实验室某生锈铁片中铁元素的质量分数,两位同学分别设计了如下甲、乙两个实验方案。方案甲:称得生锈铁片的质量为 m1g,按图 I 所示装置进行实验。完全反应后,测得室温下产生氢气的体积为 V1L,查得其密度为p1g/L。方案乙:称得生锈铁片的质量为 m2g,先按图Ⅱ所示装置进行实验。当生锈铁片完全变成光亮的银白色时,停止加热,继续通入CO至室温。取出铁片,按图 I 所示装置继续进行实验。完全反应后,测得室温下产生氢气的体积为 V2L,查得其密度为 p2g/L。
已知:Fe2O3+6HCl=2FeCl3+3H2O(FeCl3可溶于水)
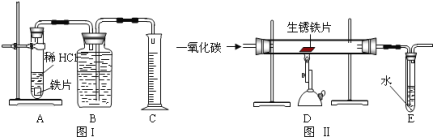
(1)铁锈的成分是__________.
(2)(评价交流)上述两个方案中,可行的是____(填“甲”或“乙”);分析不可行方案,其缺陷是____________________。
(3)(设计实验)方案乙中,同学们设计了如下实验报告,请帮助完成表中空格。
实验编号 | 实验步骤 | 实验现象 | 结论或化学方程式 |
①装置Ⅱ | 通入CO,加热.完全反应后,停止加热,继续通CO至室温 | 生锈铁片变成光亮的银白色 | CO具有______性; 化学方程式:_______ |
②装置Ⅰ | 将光亮铁片放入稀盐酸中,完全反应 | ______ |
(4)图Ⅱ所示装置有缺陷,应如何改进__________。
(5)(结论)生锈铁片中铁元素的质量分数是_________(用字母表示)。
(6)(发散)实验室经常用一氧化碳来炼铁,实验室炼的铁和工业炼的铁本质区别是_______________