��Ŀ����
�����д����л�ѧ��С����ѧ���Ļ�ѧ֪ʶ���������У���������̽����
��1����ͼ��ʾ��С����һֻ���ʼ�������ʢˮ�IJ������У���������ˮ��(���ǵ���Ҫ�ɷ���̼���)�������������μ�Ũ���ᣬ�����DZ��潫���ֵ������� ����Ӧ�Ļ�ѧ��Ӧ����ʽΪ ��

��2��С��ͬѧ�ڼ���������ͼ��ʾ��Сʵ�顣
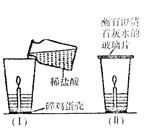
��ͼ���й۲쵽����Ҫ�����Ǽ����DZ��������ݲ������������Ϩ���ɴ˵ó��й�CO2���ʵĽ����� ��
������������ȷ��CO2��һ����Ҫ��;�� ��
�ڵ�����Ϩ����ڲ�������Ѹ�ٸǡ���պ��ʯ��ˮ�IJ���Ƭ(��ͼ��)���۲쵽�������Dz���Ƭ�ϵ�ʯ��ˮ ��������˵���ڱ����� ���������д��������ʯ��ˮ��Ӧ�Ļ�ѧ����ʽ ��
��3��С���Ѻ�̼���85���ļ�����20g��������ϡ���ᷴӦ����������������Ƕ��ٿ�?
��1����ͼ��ʾ��С����һֻ���ʼ�������ʢˮ�IJ������У���������ˮ��(���ǵ���Ҫ�ɷ���̼���)�������������μ�Ũ���ᣬ�����DZ��潫���ֵ������� ����Ӧ�Ļ�ѧ��Ӧ����ʽΪ ��

��2��С��ͬѧ�ڼ���������ͼ��ʾ��Сʵ�顣

��ͼ���й۲쵽����Ҫ�����Ǽ����DZ��������ݲ������������Ϩ���ɴ˵ó��й�CO2���ʵĽ����� ��
������������ȷ��CO2��һ����Ҫ��;�� ��
�ڵ�����Ϩ����ڲ�������Ѹ�ٸǡ���պ��ʯ��ˮ�IJ���Ƭ(��ͼ��)���۲쵽�������Dz���Ƭ�ϵ�ʯ��ˮ ��������˵���ڱ����� ���������д��������ʯ��ˮ��Ӧ�Ļ�ѧ����ʽ ��
��3��С���Ѻ�̼���85���ļ�����20g��������ϡ���ᷴӦ����������������Ƕ��ٿ�?
(1) �����DZ��������ɫ���ݣ� CaCO3+2HCl��CaCl2+CO2��+H2O��
(2) �ٶ�����̼��֧��ȼ�ա�Ҳ����ȼ�ա�����ͬ�������ܶȱȿ�����
������̼���������
�ڱ���ǡ�������̼��CO2+Ca(OH)2��CaCO3��+H2O��
(3) 7.48g
(2) �ٶ�����̼��֧��ȼ�ա�Ҳ����ȼ�ա�����ͬ�������ܶȱȿ�����
������̼���������
�ڱ���ǡ�������̼��CO2+Ca(OH)2��CaCO3��+H2O��
(3) 7.48g
��1��̼����������ᷴӦ�����Ȼ��ơ�ˮ�Ͷ�����̼�����DZ����������ݣ���������DZ��������ɫ���ݣ� CaCO3+2HCl=CaCl2+CO2��+H2O��
��2�����������Ϩ��˵��������̼�Ȳ�ȼ��Ҳ��֧��ȼ�գ��ܶȱȿ�������������𣬹��������̼��֧��ȼ�ա�Ҳ����ȼ�ա�����ͬ�������ܶȱȿ�����
������̼���������
�ڶ�����̼�����������Ʒ�Ӧ����̼��ƺ�ˮ��ʹʯ��ˮ����ǣ��������ǡ�������̼��CO2+Ca(OH)2��CaCO3��+H2O��
��3���⣺����������������Ϊx
̼��Ƶ�����=20g��85%=17g (1��)
CaCO3 + 2HCl �� CaCl2 + CO2��+ H2O
100 44
17g x ������ ����1�֣�
100/44 ��17g/x �������������� ��1�֣�
X��7.48g �������������� ��1�֣�
�𣺲�����CO2���������Ϊ7.48g
��2�����������Ϩ��˵��������̼�Ȳ�ȼ��Ҳ��֧��ȼ�գ��ܶȱȿ�������������𣬹��������̼��֧��ȼ�ա�Ҳ����ȼ�ա�����ͬ�������ܶȱȿ�����
������̼���������
�ڶ�����̼�����������Ʒ�Ӧ����̼��ƺ�ˮ��ʹʯ��ˮ����ǣ��������ǡ�������̼��CO2+Ca(OH)2��CaCO3��+H2O��
��3���⣺����������������Ϊx
̼��Ƶ�����=20g��85%=17g (1��)
CaCO3 + 2HCl �� CaCl2 + CO2��+ H2O
100 44
17g x ������ ����1�֣�
100/44 ��17g/x �������������� ��1�֣�
X��7.48g �������������� ��1�֣�
�𣺲�����CO2���������Ϊ7.48g

��ϰ��ϵ�д�
�����Ŀ