题目内容
(6分)某化工厂用氢氧化钠溶液来吸收废气中的二氧化硫,有效地防止了酸雨的形成(假定废气中只有二氧硫能与氢氧化钠溶液反应、且二氧化硫与氢氧化钠溶液反应完全。反应的化学方程式为:SO2+2NaOH=Na2SO3+H2O)。该化工厂每天消耗8t质量分数为10%的氢氧化钠溶液。
(1)8t质量分数为10%的氢氧化钠溶液中含氢氧化钠_________t。
(2)求:该化工厂每天吸收的二氧化硫的质量。

(1)8t质量分数为10%的氢氧化钠溶液中含氢氧化钠_________t。
(2)求:该化工厂每天吸收的二氧化硫的质量。

(1)0.8 (2)0.64t
(1)据溶液的质量及质量分数来计算溶质的质量,(2)根据氢氧化钠的质量,列比例就得二氧化硫的质量
(1)0.8……………………(2分)
(2)解:设该化工厂每天吸收的二氧化硫的质量为x。
SO2+2NaOH=Na2SO3+H2O
64 80……………………………………………1分
x 0.8t……………………………………………1分
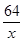 =
=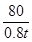 ……………………………………………1分
……………………………………………1分
x=0.64t………………………………………………1分
答:该化工厂每天吸收0.64t二氧化硫。
(1)0.8……………………(2分)
(2)解:设该化工厂每天吸收的二氧化硫的质量为x。
SO2+2NaOH=Na2SO3+H2O
64 80……………………………………………1分
x 0.8t……………………………………………1分
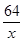 =
=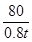 ……………………………………………1分
……………………………………………1分x=0.64t………………………………………………1分
答:该化工厂每天吸收0.64t二氧化硫。

练习册系列答案
相关题目