题目内容
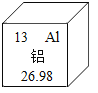
【题目】铝元素的相关信息如图所示,下列叙述正确的是( )
A.铝原子的最外层电子数为 3B.铝原子的核内中子数为 13
C.铝是地壳中含量最高的元素D.自然界中铝主要以单质形式存在
【答案】A
【解析】
A、元素周期表中的一格可以获得的信息:左上角的数字表示原子序数;原子序数=质子数=核外电子数,铝原子核外电子数为13,根据核外电子排布规律可知,铝原子的铝原子的最外层电子数为 3,故A正确;
B、元素周期表中的一格可以获得的信息:左上角的数字表示原子序数;原子序数=质子数=核外电子数,相对原子质量≈质子数+中子数,根据此图确定铝原子的核内中子数约为:27-13=14,故B错误;
C、氧是地壳中含量最高的元素,铝是地壳中含量最高的金属元素,故C错误;
D、铝化学性质较活泼,自然界中铝主要以化合物形式存在,故D错误。故选A。

练习册系列答案
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案 导学教程高中新课标系列答案
导学教程高中新课标系列答案
相关题目
【题目】为测定CuCl2和FeCl2组成的混合溶液中FeCl2的质量分数,进行如下实验:
①取200g混合溶液加入足量的AgNO3溶液,经过滤、洗涤、干燥、称量,得到143. 5gAgCl固体;
②另取原混合溶液各200g与含有杂质的废铁屑反应(杂质不溶于水,也不参与反应),共做了五组实验,其实验数据如下表。
实验组别 | 一 | 二 | 三 | 四 | 五 |
混合溶液质量/g | 200 | 200 | 200 | 200 | 200 |
铁屑质量/g | 6 | 9 | 12 | 15 | 18 |
析出铜的质量/g | 6.4 | 9.6 | m | 16 | 16 |
请分析计算:
(1)表中第三组实验的m值为____________。
(2)第___________组实验恰好完全反应。
(3)原混合溶液中FeCl2的质量分数为_________? (计算结果精确到 0.1%)