题目内容
【题目】某同学将光亮的镁条放入滴有酚酞的 NaHCO3 饱和溶液中,产生大量气泡和白色固体,溶液红色加深。点燃产生的气体,火焰淡蓝色;将燃烧产物通入澄清石灰水中,无现象。过滤,将白色固体洗净、干燥。
(1)溶液红色加深,则反应后溶液的碱性_____(填“增强”、“不变”或“减弱”)。
(2)则该气体为_____(写化学式)。
(3)为确定白色固体的成分,该同学进行了如下的探究。
(查阅资料)Mg(HCO3)2 能溶于水;MgCO3、Mg(OH)2 加热易分解,都生成两种氧化物。
(提出猜测)白色固体是:Ⅰ.MgCO3;Ⅱ__________;Ⅲ.MgCO3和 Mg(OH)2。
(进行实验)
操作 | 现象 | 结论 |
①取白色固体于试管中,加入足量的稀盐酸 | 产生气泡,固体溶解 | 白色固体中一定含有_________(写名称) |
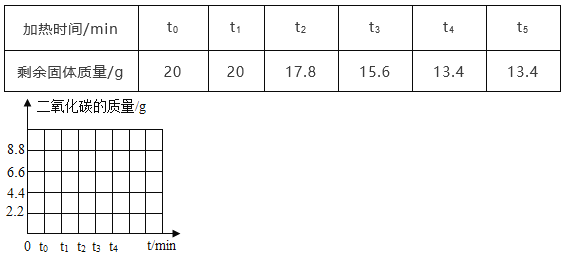
②称取干燥的白色固体 22.6 g 放在石棉网上充分加热 | 固体质量减少 |
(结论分析)
(4)据上述实验现象,小明认为猜想Ⅰ正确。但有同学认为小明的判断不严谨,因为猜想____也有相同现象。
(5)步骤①一定发生反应的化学方程式为:_____________________________。
(6)如要要确定白色固体的组成,还需要补充的操作是_____________________,再通过_______得出结论。
【答案】增强 H2 Mg(OH)2 MgCO3 Ⅲ MgCO3+2HCl=MgCl2+CO2![]() +H2O 将实验②产生的气体依次通入浓硫酸和碱石灰中,称量浓硫酸和碱石灰变化的质量 质量守恒定律计算
+H2O 将实验②产生的气体依次通入浓硫酸和碱石灰中,称量浓硫酸和碱石灰变化的质量 质量守恒定律计算
【解析】
(1)溶液红色加深,则反应后溶液的碱性增强.
(2)点燃产生的气体,火焰淡蓝色;将燃烧产物通入澄清石灰水中,无现象.则该气体为氢气,氢气的化学式是H2.
(3)白色固体可能是MgCO3,白色固体可能是Mg(OH)2,白色固体可能是MgCO3和Mg(OH)2;
①MgCO3、Mg(OH)2 加热易分解,都生成两种氧化物。MgCO3加热分解为氧化镁和二氧化碳,Mg(OH)2 加热分解为氧化镁和水,固体质量均减少,取洗净后的白色固体,加入足量的稀盐酸溶液,观察到有气泡产生,则白色固体一定含有MgCO3;
②该白色固体可以与稀盐酸反应产生气泡,则该白色固体一定含有MgCO3;
(4)根据上述实验现象可以得出,固体中一定含有碳酸镁,不能确定氢氧化镁是否存在,因为猜想Ⅲ也有相同现象;
(5)步骤①得出固体中一定含有碳酸镁,MgCO3与稀盐酸反应生成氯化镁、二氧化碳和水,方程式为:MgCO3+2HCl=MgCl2+CO2![]() +H2O;
+H2O;
(6)如要要确定白色固体的组成,还需要补充的操作是将实验②产生的气体依次通入浓硫酸和碱石灰中,称量浓硫酸和碱石灰变化的质量,从而确定生成的水和二氧化碳的质量,再通过质量守恒定律确定固体成分。

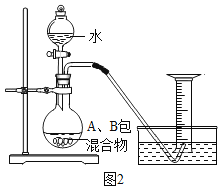
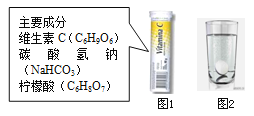
【题目】某研究小组发现,维C泡腾片(保健药品,主要成分见图1)溶于水,有许多气泡产生(如图2)。该小组同学进行如下探究。
探究一:该气体的成分
(猜想与假设)
小华说:该气体可能是CO2、O2、CO、H2、N2
小明说:不可能含有N2,因为_____。
小芳说:不可能含有CO和H2,因为从药品安全角度考虑,H2易燃易爆,CO_____。
该小组同学认为:该气体可能含有CO2、O2中的一种或两种。
(进行实验)
实验编号 | 实验操作 | 实验现象 |
① | 将气体通入澄清的石灰中 | 澄清石灰变浑浊 |
② | 将带火星的木条伸入该气体中 | 带火星的木条没有复燃 |
(得出结论)(1)由实验①可知,该气体中肯定含有_____。
(2)由实验②_____(填“能”或“不能”)确定该气体中不含氧气。
探究二:CO2的部分性质:①CO2能灭火,其灭火原理是_____。
②已知在化学反应中化合价升高的物质具有还原性,化合价降低的物质具有氧化性,H2、C、CO在夺氧的过程中化合价均升高,所以有还原性,则在反应CO2+C![]() 2CO中,CO2具有_____性。
2CO中,CO2具有_____性。
③查阅资料发现Mg能在CO2中燃烧,由此给你启发是_____。